К.т.н., доц.
Чекушина Т.В.1, д.т.н., проф. Воробьев А.Е.2, Чекушина
Е.В.1
1Институт проблем комплексного освоения недр РАН, г.
Москва, Россия
2Российский университет дружбы народов, г. Москва,
Россия
АНАЛИЗ УСЛОВИЙ ОБРАЗОВАНИЯ, МИГРАЦИИ
И НАКОПЛЕНИЯ ГАЗОСОДЕРЖАЩИХ ПОДЗЕМНЫХ ВОД
Периодически
возникающие энергетические кризисы, охватывающие многие страны мира, с особой
остротой выдвигают проблему поиска дополнительных источников энергетического
сырья. Такими нетрадиционными источниками могут стать растворенные горючие газы
подземных и морских (океанических) вод [1, 8, 9]. При этом необходимо учитывать
и то, что в подземных водах, а также водах океанов, морей и озер по всему миру
растворено значительное количество метана, и это содержание метана иногда
представляет определенный промышленный интерес. Среднее содержание метана в
водах Мирового океана составляет порядок 10-2 см3/л, а
его общее количество – 14×1012 м3.
Различные
геолого-экономические условия нахождения ресурсов растворенных газов
предполагает проведение конкретных исследований в области разработки
соответствующим этим условиям разнообразных высокоэффективных технологий
извлечения газов, представляющих практический интерес для национальной
экономики.
В этой связи, первоначально
в ходе исследований, на основе сопоставительного и контрастного изучения и сравнения, были проанализированы и
сравнены между собой существующие теоретические модели воды (с представлением
их графического изображения - электронное облако, тетраэдр, пирамида, решетка,
кластер, клатрат, топологические цепочки и кольцо, кристаллы и т.д.),
обуславливающие не только значения угла наклона между ее орбиталями атомов и
параметры (вид и характеристику) связей между ними, по величине возможного
газонасыщения и содержания (включения) ионов некоторых загрязнителей.
В настоящее время на модель структуры жидкой воды не
существует единой (общепринятой) точки зрения [4].
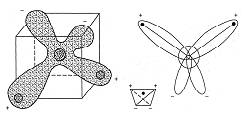
Физическую форму молекулы воды Н2О можно
рассмотреть в виде особого электронного облака (рис. 1): атом кислорода
находится в центре данного облака, а два атома водорода (с положительными
зарядами) расположены в противоположных углах нижней грани условно взятого
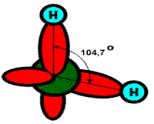
куба. При этом угол между электронными орбиталями атомов водорода в молекуле
воды равен 104,523º (рис. 2).
|
251658240 |
251658240 |
|
Рисунок 1 - Электронные орбитали и тетраэдрическая структура
молекулы воды [3] |
Рисунок 2 – Угол между атомами водорода в молекуле
воды |
Расстояние между кислородным атомом и водородными
атомами приблизительно равно 0,1 нм (0,9572·10-8 см). Причем, атом
кислорода имеет 8 электронов [3]: 2 из них расположены с
ядром, еще 2 электрона присутствуют как связка с атомами водорода в молекуле
воды, а два остальных представляют собой не поделенные пары электронов, образуя
своего рода «ветви», простираемые к верхним углам грани условного куба.
Атомы кислорода и водорода связаны между собой
ковалентно (Н – О), поэтому молекула воды обычно чрезвычайно устойчива. Составляющие молекулу воды атомы имеют малые атомные
радиусы, вследствие чего, длина Н-О связи в ее молекуле составляет всего 0,096
нм [3]. Причем, наибольший размер молекулы
воды имеет значение около 3 ангстрем.
В связи с указанным распределением положительного и
отрицательного зарядов в молекуле воды существует большой дипольный момент,
который имеет основное значение при взаимодействии таких молекул между собой, а
также и с растворенными веществами.
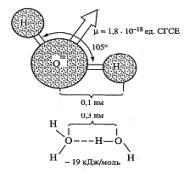
Таким образом, возникают водородные связи между
молекулами воды. Их энергия составляет порядка 1 кДж/г, а длина связи
(расстояние между атомами кислорода до двух соседних молекул) равна 0,3 нм
(рис. 3).
|
251658240 |
Рисунок 3 - Схематическое
изображение структурных особенностей молекулы воды и водородной связи [3] |
Имеющимися
особенностями строения молекул воды и ее структуры объективно объясняется
существующие изменения электропроводности водных растворов (позволяющие полезно
использовать этот эффект при последующем теоретическом обосновании и практической
реализации выделения газов, а также очистки вод от загрязнителей), а также пропорциональное
уменьшение вязкости вод, при повышении пластового давления (что способствует
уточнению математической модели образования, миграции и накопления газоносных
подземных вод) и другие ее свойства (табл. 1).
Растворенные в воде
вещества, заполняя пространство внутри кристаллической решетки воды, обычно
изменяют ее изначальную структуру и свойства. В частности, электропроводность
водных растворов, как правило, увеличивается в десятки тысяч раз (благодаря
появлению заряженных ионов в воде). Кроме этого, пропорциональное уменьшение
вязкости воды происходит с увеличением температуры и давления, что делает ее
довольно подвижной [2] даже в глубоких водоносных горизонтах (с очень высокими
пластовыми давлениями).
Для последующей
разработки эффективных методов дегазации подземных вод важным представляется и
коэффициент поверхностного натяжения, при 0ºС имеющий значение 75,65×10-3
Н/м. При разработке эффективных методов выделения водорастворимых газов
необходимо учитывать, что размеры молекул воды обычно меньше молекул и ионов
всех растворенных, коллоидов и неионогенных веществ находящихся в ней (табл.
2).
Таблица 1 - Свойства
воды [4]
|
Свойства жидкой воды,
насыщенного пара |
Изменение свойств с
ростом температуры и давления вдоль двухфазной кривой жидкость - насыщенный
пар |
Сравнительная
характеристика |
|
Плотность воды, г/см3
– 0,998 Насыщенного пара, г/дм3,
при 20 ºС 0,0173 |
Плотность
жидкой воды уменьшается, плотность насыщенного пара возрастает, достигая
0,322 г/см3 в критической точке (374ºС и 22,1 МПа) |
С
увеличением солености до 300 г/кг плотность увеличивается до 1,2-1,3 г/см3
в зависимости от состава водного раствора |
|
Теплоемкость при 0ºС, воды –
4,22, пара 1,87 |
Для жидкой воды
проходит через минимум, для пара возрастает |
Высокая по сравнению
с другими веществами |
|
Скрытая теплота плавления льда,
кДж/г 0,3 |
|
|
|
Скрытая теплота испарения воды
при 100ºС, кДж/г, 2,26 |
Убывает, стремясь к
нулю критической точке |
|
|
Коэффициент объемного расширения,
град-1, при 0ºС -3,4×10-5
при 10ºС 9×10-5 |
Температура
максимальной плотности для чистой воды 4 ºС |
Температура
максимальной плотности уменьшается с повышением солености |
|
Коэффициент поверхностного
натяжения, при 0 ºС, Н/м 75,65×10-3 |
Убывает, стремясь к
нулю в критической точке |
Высокий по сравнению
с другими жидкостями |
|
Вязкость при 0ºС,
мкПа×с 1,792 |
Уменьшается с
температурой |
С ростом солености
возрастает |
|
Диэлектрическая проницаемость при
25 ºС, 78,3 |
Уменьшается с
температурой |
Наиболее высокая для
жидкостей |
|
Электролитическая диссоциация при
25 ºС, г-ион, Н+ и СН- в кг воды, 10-7 |
Для жидкой воды
проходит через максимум |
При сверхкритических
параметрах убывает с температурой и возрастает с давлением |
|
Электропроводность при 0ºС, Ом-1, м-1,
0,68×106 |
Возрастает с
температурой |
Резко возрастает при
растворении неорганических веществ |
|
Теплопроводность при 0ºС,
МВт×м-1× град-1 , 561 |
Уменьшается с
температурой |
Наиболее высокая для
жидкостей |
|
Растворяющая способность |
Увеличивается для
сильных электролитов (галит, сильвин), проходит через максимум для многих
оксидов (кварц и др.) убывает для сульфатов, карбонатов |
Вода обладает
наиболее высокой растворяющей способностью к неорганическим веществам благодаря
высокой диэлектрической проницаемости |
|
Прозрачность |
|
Относительно высока |
Рассмотренные характеристики и показатели воды
оказывают существенное влияние на последующие процессы формирования природных
вод в литосфере.
В настоящее время существует две основные теории
образовании воды (современная земная гидросфера оценивается величиной
1,385×109 км3) на нашей планете – литогенетическая
(обусловленная химическим синтезом воды в недрах Земли) и биогенетическая
(вследствие биохимического синтеза воды живым веществом).
Таблица 2 - Диаметр молекул
некоторых газов [4]
|
Название вещества |
Критический размер молекул
веществ, нм |
Название вещества |
Критический размер молекул
веществ, нм |
|
Гелий |
0,22 |
Хлородифторметан |
0,49 |
|
Аргон |
0,34 |
Дихлородифторметан |
0,49 |
|
Ацетилен |
0,24 |
Пропан |
0,49 |
|
Водород |
0,27 |
бутан и высшие n-парафины |
0,49 |
|
Вода (H2O)
|
0,28 |
Диоксид углерода |
0,40 |
|
Этил
меркаптан |
1 |
i-бутан и высшие i-парафины |
0,56 |
|
Моноксид углерода |
0,39 |
Азот |
0,35 |
|
Метил меркаптан |
0,45 |
Циклогексан |
0,61 |
|
Метан |
0,39 |
Хлор (Cl2) |
0,49 |
|
Сульфид водорода |
0,36 |
Кислород |
0,26 |
|
Полипропилен |
0,50 |
Этилен |
0,42 |
|
Этан |
0,44 |
Бензол |
0,58 |
|
Диоксид серы (SO2) |
0.34 |
|
|
Платон и Аристотель первыми пытались объяснить происхождение подземных
вод [2]. В частности, Платон (427-347 гг. до н.э.) предположил, что их
образование происходит на основе морских соленых вод, которые, проходя горные
породы, освобождаются от солей и выходят на дневную поверхность уже пресными
родниками. По мнению Аристотеля (384-322 гг. до н.э.) образование подземных вод
происходит в результате сгущения холодного воздуха в имеющихся под землей
пустотах горных пород.
К настоящему времени разработана базовая классификация подземных вод по
их происхождению.
Ювенильные воды
накапливаются в расплавленной магме в виде паров, где их содержание составляет от 0,5 до 8,01% [2]. Проходя
во время извержений вулканов через охлажденную земную кору, эти воды достигают
дневной поверхности и начинают конденсироваться (теория Зюсса).
По подсчетам Семененко
Н.П., за всю историю существования Земли на ее поверхность выделилось около
3,4×109 км3 ювенильных вод.
В самом начале ХХ века Андрусовым Н.И., Гефером Г. и Лейном А.Ч.
независимо друг от друга была выдвинута гипотеза седиментогенного происхождения подземных
вод. В ее основе лежало «захоронение» морских вод при образовании донных
осадков и их последующее «отжатие» при уплотнении массива горных пород.
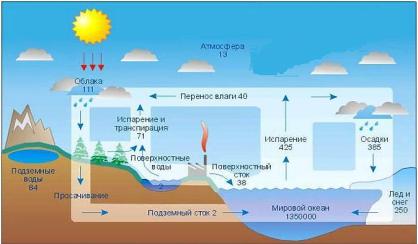
Необходимо отметить,
что в соответствии с современными воззрениями атмосферные воды (осадки)
являются первой стадией формирования поверхностных и подземных вод (рис. 4).
|
251658240 |
Рисунок 3 - Круговорот
воды в природе |
Конденсационные и
инфильтрационные воды называются метеорными или вадозными (от лат. Vadere
— идти, двигаться), т.к. они образуются из влаги атмосферы и также
участвуют в общем круговороте воды [6,7].
Формирование подземных вод
происходит за счет атмосферных осадков,
просачивающихся в последующем вглубь
литосферы, а также из болот, рек, озер и водохранилищ. Эти воды проникают в
массивы проницаемых горных пород, доходят где-то до водоупорного слоя и
накапливаются над ним. Количество влаги, таким образом, проникающей сначала в
почву, а затем далее – в литосферу, составляет 15-20% общего количества атмосферных
осадков. В одних блоках литосферы воды просачиваются довольно глубоко, а в других
- часто не проходят глубже почвенного слоя или первого водоупорного горизонта.
На степень
инфильтрации вод значительное влияние оказывает рельеф местности, состав
покрывающих пород и степень обнаженности коренных пород, их литологический
состав, структура и текстура, а также и тектоническое строение района [9].
Зачастую на интенсивность инфильтрации вод влияет имеющийся растительный покров
и техногенная деятельность.
Нами был осуществлен
детальный анализ условий образования, миграции и накопления газосодержащих
подземных вод на основе
теоретического и экспериментального изучения к настоящему времени уже известных
или потенциально возможных характеристик и параметров различных
гидрогеологических бассейнов.
Литература
1.
Технология извлечения метана, деминерализация
подземных и промышленных вод /Воробьев А.Е., Портнов В.С., Роман А.Т., Таткеева
Г.Г., Турсунбаева А.К. – Караганда: Издательско-полиграфический центр
Казахстанско-Российского университета. 2012.-
320 с.
2. Зверев
В.П. Подземные воды земной коры и геологические процессы. – М.: Научный мир. –
2006. – 256 с.
3.
Климентов
П.П. Гидрогеология. М., Госгеолтехиздат, 1955.
4.
Крайнов
С.Р., Швец В.М. Гидрогеохимия. М.: Недра, 1992, 463 с.
5.
http://greensource.ru/istochniki-jenergii/podzemnye-vody.html.
6.
http://www.geohydrology.ru/gazyi-v-podzemnyih-vodah.html.
8.
Стратегия
развития минерально-сырьевого комплекса в XXI веке //Материалы II Междунар.
конф., [г. Москва, 11-15 окт. 2006 г.] / отв. ред. - А. Е. Воробьев. Москва,
2006.
9.
Воробьев
А.Е., Роман А.Т., Нуршина А.Р. и др. Применение мембранной абсорбции - основной
метод выделения газа из подземных вод // Материалы Х Междунар. конф. «Ресурсовоспроизводящие,
малоотходные и природоохранные технологии освоения недр». – Москва: РУДН, 2011.
- С. 40-41.