Кравченко С.В., Бурковский Р.П.
Днепропетровский
государственный аграрно-экономический университет,
ул. Ворошилова, 25, Днепропетровск
49600, Украина
синтез
и строение n-гидрокси-3,6-ЭНДО-метилен-1,2,3,6-тетрагидрофталимида
Взаимодействие фталевого ангидрида с
гидроксиламином является удобным и селективным способом получения N-гидроксифталимида. Однако
продукту взаимодействия 3,6-эндо-метилен-1,2,3,6-тетрагидрофталевого
ангидрида (эндикового ангидрида) с гидроксиламином в
среде метанола на основании данных спектра ЯМР 1Н приписана
структура 1,4-диоксо-5,8-эндо-метилен-3,8,9,10-тетрагидробенз-2,3-оксазина 2 [1]:
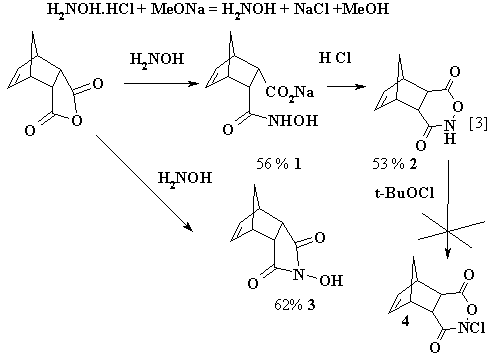
Первоначальный продукт взаимодействия эндикового ангидрида с гидроксиламином
авторы работы [1] постулировали как Na-соль 1,
подкисление которой приводит к образованию 2,3-оксазина 2 [1]. Однако
возникает вопрос, каким образом при взаимодействии 3,88 г (55,827 ммоль) H2NOH·HCl с раствором 1,28 г (55,652 г-атом) металлического Na в метаноле, то есть с 55,652 ммоль MeONa, может образоваться Na-соль 1.
Ведь весь MeONa
переводится при этом в 55,652 ммоль NaCl.
Доказательство структуры 2,3-оксазина 2 с помощью только данных спектра ЯМР 1Н тоже нельзя
признать строгим и тем более однозначным.
Продолжая наши
предыдущие исследования в области N-хлор-N-ацилоксиамидов [2], мы
осуществили взаимодействие свежесублимированного в вакууме 3,6-эндо-метилен-1,2,3,6-тетрагидрофталевого
ангидрида (эндикового ангидрида) с гидроксиламином в
среде метанола и полученный продукт (бесцветные кристаллы с т.пл. 163 – 164 °С (в работе [1] т.пл. 160 °С) попытались прохлорировать по атому азота трет-бутилгипохлоритом [2]. Однако получить ожидаемое N-хлорпроизводное
4 не удалось – хлорирование по
атому азота не наблюдалось.
Подробное изучение строения продукта взаимодействия эндикового
ангидрида с гидроксиламином с помощью ЯМР 1Н спектроскопии,
масс-спектрометрии и РСА показало, что он является N-гидрокси-3,6-эндо-метилен-1,2,3,6-тетрагидрофталимидом,
как и следовало ожидать из классических представлений органической химии.
В спектре ЯМР 1Н присутствуют два дублета АВ (1.496 и 1.585,
2J = 8,4 Гц) протонов метиленовой группы, два близко
расположенных синглета протонов у третичных атомов углерода – при 3,252 м.д. (С(3)Н,С(6)Н) и при 3,265 м.д. (С(1)Н,
С(2)Н); синглет протонов у двойной связи при 6,063 м.д. (С(4)Н, С(5)Н), а также синглет кислого протона связи NOH при 10,557 м.д. Подобные значения сдвигов протона
связи NOH характерны для
3-гидрокси-5-арилимидазолидин-2,4-дионов (3-N-гидрокси-5-арилгидантоинов), в которых группа NOH так же находится между двумя группами С=О [3]. Кроме
того, данные спектра ЯМР 1Н свидетельствуют о симметричности
структуры соединения 3, что
невозможно для структуры 2.
В масс-спектре соединения 3
присутствует пик иона с m/z 180 [M+H]+ (100%).
Структура соединения 3
однозначно подтверждается также данными РСА (рис. 1, табл. 1, 2).
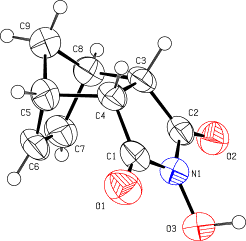
Рис. 1. Строение N-гидрокси-3,6-эндо-метилен-1,2,3,6- тетрагидрофталимида 3
согласно данным РСА
Нонборнановый и пирролидиновый
циклы сочленены по цис-типу (торсионный угол H3-C3-C4-H4 0 град.,
пирролидиновый цикл имеет транс-
ориентацию относительно метиленового мостика нонборнана (торсионный угол
С9-С8-С3-С2 151.04(13) град.) Атом азота N(1) имеет очень слабопирамидальную, почти плоскую
конфигурацию, параметр пирамидальности Винклера – Дунитца [4] 171°, сумма
валетных углов у атома N(1) составляет
359,37 град. В кристалле молекулы 3
связаны в двойные цепочки вдоль оси b
межмолекулярными водородными связями O3-H3…O2i [i: 1-x,1/2+y,1/2-z]
(H…O 1.69(3) Å, O-H…O 176(2) град.) и C8-H8…O2ii [ii: 1-x,-1/2+y,1/2-z]
(H…O 2.55 Å, C-H…O 155 град.).
Таблица 1
Длина связей в Å в соединении 3
|
Связь |
Длина, Å |
Связь |
Длина, Å |
|
O(1)–C(1) |
1,2093(19) |
C(3)–C(8) |
1,562(2) |
|
O(2)–C(2) |
1,2176(18) |
C(4)–(C(5) |
1,567(2) |
|
O(3)–N(1) |
1,3806(17) |
C(5)–C(6) |
1,503 |
|
N(1)–C(1) |
1,387(2) |
C(5)–C(9) |
1,529(2) |
|
N(1)–C(2) |
1,374(2) |
C(6)–C(7) |
1,319(3) |
|
C(1)–C(4) |
1,496(2) |
C(7)–C(8) |
1,513(2) |
|
C(2)–C(3) |
1,493(2) |
C(8)–C(9) |
1,533(2) |
|
C(3)–C(4) |
1,537(2) |
|
|
Таблица 2
Валентные углы (град.) в соединении 3
|
Угол |
Градус |
Угол |
Градус |
|
O(3)–N(1)–C(1) |
121,94(13) |
C(1)–C(4)–C(3) |
105,80(13) |
|
C(2)–N(1)–O(3) |
122,18(14) |
C(1)–C(4)–C(5) |
114,38(13) |
|
C(2)–N(1)–C(1) |
115,25(14) |
C(3)–C(4)–C(5) |
102,81(13) |
|
O(1)–C(1)–N(1) |
123,76(16) |
C(6)–C(5)–C(4) |
106,25(14) |
|
O(1)–C(1)–C(4) |
129,79(160 |
C(6)–C(5)–C(9) |
100,39(15) |
|
N(1)–C(1)–C(4) |
106,45(13) |
C(9)–C(5)–C(4) |
99,40(13) |
|
O(2)–C(2)–N(1) |
123,16(16) |
C(7)–C(6)–C(5) |
107,95(15) |
|
O(2)–C(2)–C(3) |
129,36(15) |
C(6)–C(7)–C(8) |
107,78(16) |
|
N(1)–C(2)–C(3) |
107,47(13) |
C(7)–C(8)–C(3) |
106,31(13) |
|
C(2)–C(3)–C(4) |
105,02(13) |
C(7)–C(8)–C(9) |
100,10(15) |
|
C(2)–C(3)–C(8) |
114,39(13) |
C(9)–C(8)–C(3) |
98,99(13) |
|
C(4)–C(3)–C(8) |
103,30(12) |
C(5)–C(9)–C(8) |
94,25(13) |
N-Гидрокси-3,6-эндо-метилен-1,2,3,6-тетрагидрофталимид
3 подобно N-гидроксифталимиду [5] может иметь важное промышленное значение в
качестве сокатализатора окисления алкановых компонентов нефти до спиртов,
кетонов и кислот кислородом воздуха при комнатной температуре.
Библиографические ссылки
1. Syhthesis of 1,4-dioxo-5,8-endomethylene-3,8,9,10-tetrahydrobenz-2,3-oxazine from 3,6-endomethylene-1,2,3,6-tetrahydrophtalic anhydride / V.A. Slavinskaya, Dzh. Sile, E. Kh. Korchagova et al. // Chem. Heterocycl. Comp. – 1995. – Vol. 31, № 3. – P. 366.
2. Кравченко С.В. N-Хлор-N-бензоилоксибензамид / С.В. Кравченко // Вісник Дніпропетр.
ун-ту. Серія «Хімія». – 2013. – Вип. 19. – С. 57 – 61.
3. Synthesis and crystal structure of new imidazolidine-2,4-dione and imidazolidin-2-one derivatives / V.G. Shtamburg, A.A. Anishchenko, V.V. Shtamburg et al. // Mendeleev Commun. – 2008. – Vol.
18. – P. 102 – 104.
4. Burgi H.B. Structure correlation. /
H.B. Burgi, J.D. Dunitz // VCH. Weinheim. – 1994. –Vol. 2. – P. 741
– 784.
5. Recupero F. Free Radical Functionalization of Organic Compounds Catalazyed by N-Hydroxyphtalimide / F. Recupero, C. Punta // Chem. Rev. –
2007. – Vol. 107. – P. 3800 – 3842.