Технические науки/11.Робототехника
Магистр
экономических наук, ст. преподаватель Летвинко П.С.
Костанайский
государственный университет им. А. Байтурсынова, Казахстан
Магистрант
Попченко А.С.
Костанайский
государственный университет им. А. Байтурсынова, Казахстан
Использование
численных методов в проектировании искусственных желудочков сердца
роторного типа
В
настоящее время комплексом мер по поддержанию замещающей функции сердца
человека при заболеваниях сердечно-сосудистой системы является механическая
поддержка кровообращения. Одним из
подходов в МПК является обход желудочка сердца, т.е. установка миниатюрного
насоса для перекачивания крови из полости желудочка в восходящий отдел аорты,
минуя артериальный клапан. Для операций подобного рода применяются осевые,
центробежные и диагональные насосы: [1,
2]. В клинической практике такие
насосы называются искусственными желудочками сердца (ИЖС). Искусственный желудочек сердца (ИЖС) –
сложное устройство, элементы которого представлены на рис. 1. Существуют
различные методы проектирования искусственного желудочка сердца роторного типа.
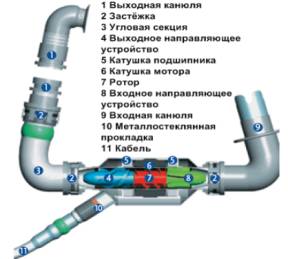
Рис. 1. Элементы ИЖС и периферии для модели INCOR
(BerlineHeart, Германия)
В
статье проведен анализ результатов численного эксперимента по проектированию
ИЖС: рассмотрены поля скоростей в области входного аппарата ИЖС.
Моделирование
поведения потока крови в проточной части ИЖС проводится с помощью Computational
Fluid Dynamics (CFD) – вычислительной гидродинамики – подраздела механики
сплошных сред, включающего совокупность физических, математических и численных
методов, предназначенных для вычисления характеристик потоковых процессов. На
начальных стадиях разработки ИЖС CFD позволяет оценить выбранную геометрию,
применяя различные численные методы решения:
·
метод
конечных объёмов;
·
метод
конечных элементов;
·
метод
сглаженных частиц;
·
метод
с использованием функции распределения вероятности.
Гидродинамический анализ
в различных модулях позволяет определить параметры движения жидкой среды, такие
как: перепад давления, распределение скоростей, направление течения, подъемная
сила и лобовое сопротивление, влияние нагрева и охлаждения. Анализ может быть
применен для расчета параметров потока, распределения давления и температуры в
однофазной вязкой жидкости.
На начальном этапе
проектирования насоса ИЖС необходимо выявить особенности поведения потока
жидкости в проточной части насоса. В
данном случае будет продемонстрирован пример расчета для области входного
аппарата (область входной канюли и спрямляющего аппарата). Входной аппарат представляет собой трубку с
несколькими лопатками прямолинейного профиля со скруглениями. В данном
исследовании рассматривается входной аппарат с 3 и 4 лопатками, что
соответствует большинству самых распространенных осевых насосов ИЖС [3, 4].
Геометрическая модель представляет собой область, в которой течет жидкость.
Стенки входной канюли и входного аппарата учитываются в виде граничных условий
(без скольжения, no slip wall). На рис. 2 представлена геометрическая модель
канюли.
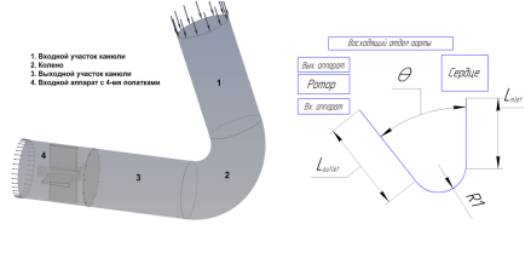
а) б)
Рис. 2. Составные части
геометрической модели (а) и основные параметры геометрии (б)
Непосредственное
моделирование гемодинамики происходит в Ansys CFD методом конечных
объемов. В ИЖС поток крови, проходящий
далеко от стенок, является турбулентным (максимальное число ![]() ), а в пристеночном слое – ламинарным, поэтому в качестве
модели турбулентности выбрана гибридная модель Shear Stress Transform Method (k-
), а в пристеночном слое – ламинарным, поэтому в качестве
модели турбулентности выбрана гибридная модель Shear Stress Transform Method (k-![]() ) [5]. Кровь задается постоянными параметрами вязкости и
плотности. Динамическая вязкость крови
) [5]. Кровь задается постоянными параметрами вязкости и
плотности. Динамическая вязкость крови ![]() 0,0035 кг/м с, что соответствует гематокриту на уровне 33%
(основной класс вероятных кандидатов на установку ИЖС). Плотность крови
0,0035 кг/м с, что соответствует гематокриту на уровне 33%
(основной класс вероятных кандидатов на установку ИЖС). Плотность крови ![]() 1050 кг/
1050 кг/![]() . Регионы 1-3 и 4 (рис.
2, а) разбиваются на конечные объемы отдельно, а потом сшиваются. Таким
образом, при генерации сетки используются различные методы разбиения, что
уменьшает результирующее количество элементов. Для обеспечения точных
результатов невязка варьировалась от
. Регионы 1-3 и 4 (рис.
2, а) разбиваются на конечные объемы отдельно, а потом сшиваются. Таким
образом, при генерации сетки используются различные методы разбиения, что
уменьшает результирующее количество элементов. Для обеспечения точных
результатов невязка варьировалась от ![]() до
до ![]() . Изменение выходных
параметров (скорость, перепад давления) менее 5 % гарантировалось уровнем
невязки
. Изменение выходных
параметров (скорость, перепад давления) менее 5 % гарантировалось уровнем
невязки ![]() . Для обеспечения качественного решения, сетка конечных
элементов сглаживалась в сеточном генераторе Ansys ICEM CFD и проверялась по
критерию качества (element quality >
0.2). Начальные параметры
геометрии: длина входного участка – 30 мм, длина выходного участка 30 мм,
радиус кривизны колена (по средней линии) – 15 мм, угол между входным и
выходным участком канюли – 70 градусов, диаметр канюли – 16 мм. Значения начальных параметров принимались
близкими к размерам, уже используемых, ИЖС (например, HeartMate [8]). Геометрия
3-х и 4-х лопаточного входного аппарата в расчетах не изменялась. В качестве
граничного условия на входе задается массовый расход 5 л/мин, что соответствует
нормальной производительности сердца.
Условие на выходе из входного аппарата – нулевое статическое давление.
. Для обеспечения качественного решения, сетка конечных
элементов сглаживалась в сеточном генераторе Ansys ICEM CFD и проверялась по
критерию качества (element quality >
0.2). Начальные параметры
геометрии: длина входного участка – 30 мм, длина выходного участка 30 мм,
радиус кривизны колена (по средней линии) – 15 мм, угол между входным и
выходным участком канюли – 70 градусов, диаметр канюли – 16 мм. Значения начальных параметров принимались
близкими к размерам, уже используемых, ИЖС (например, HeartMate [8]). Геометрия
3-х и 4-х лопаточного входного аппарата в расчетах не изменялась. В качестве
граничного условия на входе задается массовый расход 5 л/мин, что соответствует
нормальной производительности сердца.
Условие на выходе из входного аппарата – нулевое статическое давление.
На рис. 3 представлено
распределение скоростей в проточной части на срезе, проходящем по осевой линии
канюли и входного аппарата для начальных геометрических размеров.
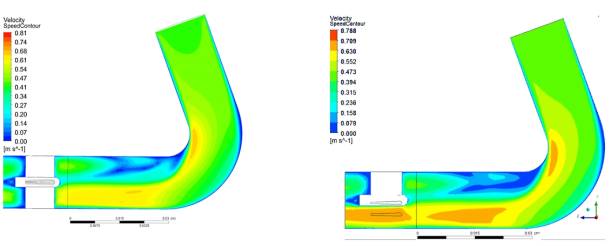
а)
б)
Рис. 3. Распределение
скоростей в проточной части для случая 4-х лопаточного входного аппарата (а),
распределение скоростей в проточной части для случая 3-х лопаточного входного
аппарата (б)
В области выходной части
канюли (зона 3, рис. 2, а) образуется зона со скоростями много меньше скоростей
основного потока. В случае клинических испытаний в этой зоне будут оседать
форменные элементы крови и образовываться тромб, который может попасть в
восходящий отдел аорты и малые кровеносные сосуды. В гидравлике это эффект известен хорошо, но он не является
существенным при проектировании. В случае осевых насосов ИЖС этот эффект
является уже критическим [6] и напрямую может повлиять на выживаемость
пациента.
В результате численного
анализа для начальной геометрии установлено, что поток, набегающий на ротор
после входного аппарата, не является симметричным (рис. 4).
Отношение максимальных
скоростей в области 2 и в области 1 для входного аппарата с 4-мя лопатками – VR4
=1,61, c 3-мя =1,56.
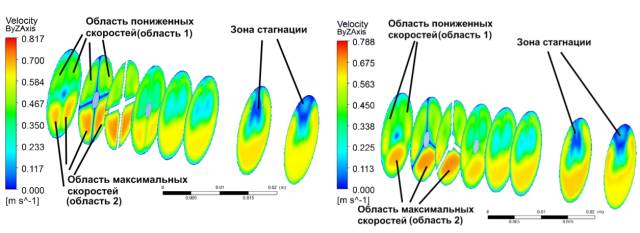
а) б)
Рис. 4. Распределение
скоростей в проточной части для случая 4-х лопаточного входного аппарата (а),
распределение скоростей в проточной части для случая 3-х лопаточного входного
аппарата (б)
При изменении увеличении
радиуса колена несимметричность потока нивелируется. Данные расчетов показаны
на рис. 5. Изменение угла колена не
приводит устранению несимметричности потока на выходе из спрямляющего
аппарата. Результаты продемонстрированы
на рис. 6. При варьировании диаметра канюли несимметричность потока пропадает в
случае малых диаметров. Изменение длины
выходного участка канюли для 4-х лопаточного спрямляющего аппарата приводит к устранению
несимметричности при увеличении длины выходного участка.
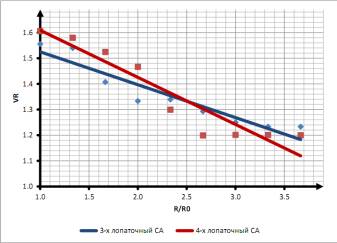
Рис. 5. Изменение
отношения максимальных скоростей VR в зависимости от безразмерного радиуса
колена канюли для 3-х и 4-х лопаточного спрямляющего аппарата (СА); R0 – 30 мм
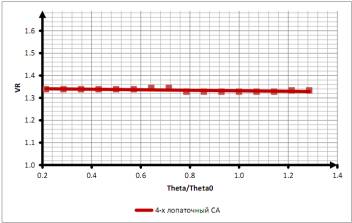
Рис. 6. Изменение
отношения максимальных скоростей VR в зависимости от безразмерного угла между
входным и выходным участком канюли 4-х лопаточного спрямляющего аппарата (СА);
Theta0 - 70 мм
Литература
1. Agarwal S., High K.M. Newer-generation ventricular assist devices //
Best Practice & Research Clinical Anaesthesiology. 2012. Vol. 26, no. 2. P.
117-130. DOI: 10.1016/j.bpa.2012.01.003
2. Milano C.A., Simeone A.A. Mechanical circulatory support: devices,
outcomes and complications // Heart Failure Reviews. 2013. Vol. 18, no. 1. P.
35-53.
3. Богданова Ю.В.,
Гуськов А.М. Особенности
проектирования устройства
искусственного желудочка сердца:
обзор работ //
Наука и образование. МГТУ им. Н.Э. Баумана. Электрон. журн. 2014. № 3. С. 162-187. DOI: 10.7463/0314.0705250
4. Hetzer R., Hennig E. Mechanical Circulatory Support Systems // In:
Springer Handbook of Medical Technology / ed. by R. Kramme, K.-P. Hoffmann,
R.S. Pozos. Springer Berlin Hei-delberg, 2011. С.
723-748. DOI:
10.1007/978-3-540-74658-4_36
5. Apel J., Neudel F., Reul H. Computational fluid dynamics and
experimental validation of a microaxial
blood pump //ASAIO
Journal. 2001. Vol.
47, no. 5.
P. 552-558. DOI: 10.1097/00002480-200109000-00031
6. Kamdar F., John R. Surgical Mechanical Circulatory Support // In:
Coronary Heart Disease / ed. by Z.
Vlodaver, R.F. Wilson,
D.J. Garry. Springer
US, 2012. С. 455-469.
DOI: 10.1007/978-1-4614-1475-9_26
7. O’Neill W.W., Schreiber T., Wohns D.H.W., Rihal C., Naidu S.S.,
Civitello A.B., Dixon S.R., Massaro J.M., Maini B., Ohman E.M. The Current Use
of Impella 2.5 in Acute Myo-cardial Infarction Complicated by Cardiogenic
Shock: Results from the USpella
Registry // Journal of Interventional
Cardiology. 2014. Vol. 27, no. 1. P. 1-11. DOI: 10.1111/joic.12080
8. Palacios I.F. Left ventricular assistant device impella 2.5 usage for
patients undergoing high risk PCI // Catheterization and Cardiovascular
Interventions. 2012. Vol. 79, no. 7. P. 1135-1137.
9. Sibbald M., Dzavik V. Severe hemolysis associated with use of the
impella LP 2.5 mechani-cal assist device // Catheterization and Cardiovascular
Interventions. 2012. Vol. 80, no. 5. P. 840-844. DOI: 10.1002/ccd.24280