Химия и химические технологии / 7. Неорганическая
химия
К.т.н Ожередова
М.А.
Технологический
институт Восточноукраинского национального университета им. В. Даля (г.
Северодонецк), Украина
Получение гидроксикарбоната никеля
из жидких
никельсодержащих отходов
Производство гидроксикарбоната никеля, имеющего
широкое потребление при производстве катализаторов, ферритов, радиокерамических
изделий, порошкообразного никеля, в строительной индустрии и
т.п., требует использования дорогостоящего никельсодержащего сырья. В условиях
ресурсной зависимости Украины от внешних источников такого сырья, возникает
необходимость в создании технологий по извлечению никеля из отходов производств
и оборотном использовании его в промышленности.
Источниками образования жидких никельсодержащих отходов являются производства
катализаторов, сверхтвёрдых материалов, неорганических пигментов, а также
предприятия металлургического комплекса. Отработанные растворы этих производств
представляют собой высококонцентрированные никельсодержащие растворы,
содержащие от 30 до 100 г/л и низкоконцентрированные - с содержанием от 50-150 мг/л солей никеля (II).
Разработанные и известные в настоящее время
технологии переработки подобных отходов не
позволяют получать легко утилизируемые продукты, и потому чаще всего их
собирают в шламонакопителях. Это приводит с одной стороны к безвозвратным
потерям никельсодержащего сырья, естественные запасы которого находятся на
грани исчерпания, а с другой – к загрязнению окружающей среды высокотоксичными
отходами.
Образование
никельсодержащих жидких отходов катализаторных и металлообрабатывающих
производств приводит к ежегодным потерям никеля до 1650 т [1]. Решение данной
экологической проблемы должно быть связано с разработкой локальной технологии
утилизации никельсодержащих отработанных растворов с получением ликвидных
продуктов, в частности гидроксикарбоната никеля.
Исследования проводили с модельными и реальными
никельсодержащими растворами.
В качестве реальных никельсодержащих растворов использовали сточные воды и отработанные высококонцентрированные растворы цеха по механической обработке изделий Николаевского ПО «Заря».
Состав сточных вод (мг/л):
раствор №1 NiSO4 – 155,0; Na2SO4
– 60,0; H3BO3 – 20,0; Fe2(SO4)3
– 10,0; pH – 5,8;
раствор № 2 NiCl2 – 160,0; НCl – 70,0; FeCl3– 10,0; pH – 3,8.
Состав реальных отработанных высококонцентрированных растворов (г/л):
раствор № 3 NiSO4 – 104,2; Na2SO4
– 60,0; H3BO3 – 20,0; Fe2(SO4)3
– 10,0; pH – 4,1;
раствор № 4 NiCl2 – 147,53; НCl – 100,0; FeCl3 – 10,0;
pH – 0,57.
Модельные растворы получали путем разбавления реальных отработанных высококонцентрированных растворов. Состав модельных растворов (г/л):
раствор № 5 NiSO4 – 34,87; Na2SO4
– 20,0; H3BO3 – 7,0; Fe2(SO4)3
– 3,5;
раствор № 6 NiSO4 – 69,59; Na2SO4
– 40,0; H3BO3 – 14,0; Fe2(SO4)3
– 7,0;
раствор № 7 NiCl2 – 49,28; НCl – 33,5; FeCl3 – 3,5;
раствор № 8 NiCl2 – 98,41; НCl – 67,0; FeCl3 – 7,0.
Осаждение
проводили с использованием в качестве осадителей насыщенных при 20 0С
растворов кальцинированной соды и троны (механическая смесь карбоната и
гидрокарбоната натрия).
В основе химического осаждения лежат термодинамически возможные реакции:
3NiSO4
+ 3Na2CO3 + 6H2O = NiCO3 × 2Ni(OH)2
× 4H2O
+3Na2SO4 +2CO2 (1)
![]() G1 = - 138,22 кДж/моль
G1 = - 138,22 кДж/моль
3NiCl2
+ 3Na2CO3 + 6H2O = NiCO3 × 2Ni(OH)2
× 4H2O
+ 6NaCl + 2CO2 (2)
![]() G2 = - 159,55 кДж/моль
G2 = - 159,55 кДж/моль
3NiSO4+2(Na2CO3×NaHCO3×2H2O)+H2O=NiCO3×2Ni(OH)2×4H2O+3Na2SO4+3CO2
(3)
![]() G3 = - 134,27 кДж/моль
G3 = - 134,27 кДж/моль
3NiCl2+2(Na2CO3×NaHCO3×2H2O)
+ H2O=NiCO3×2Ni(OH)2×4H2O+6NaCl+3CO2
(4)
![]() G4 = - 155,59 кДж/моль
G4 = - 155,59 кДж/моль
На основании
полученных экспериментальных данных было установлено, что процесс осаждения
гидроксикарбоната никеля описывается уравнением первого порядка с константой
скорости 1,2 моль/(м3∙час) – для низкоконцентрированных
растворов и 4,8 моль/(м3∙час) – для высококонцентрированных
растворов. Относительное пресыщения, которое соответствует началу образования
твердой фазы при осаждении ионов никеля (II) из низкоконцентрированных
растворов составляет 1,56, а для высококонцентрированных растворов - 1,25.
Обработкой
экспериментальных данных была получена общая математическая зависимость процесса химического
осаждения ионов никеля (ІІ) из отработанных
растворов, которая учитывает зависимость основных показателей, которые наиболее
влияют на процесс осаждения, от концентрации Ni2+:
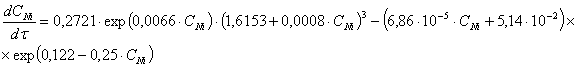
где ![]() - зависимость
константы скорости от начальной концентрации Ni2+;
- зависимость
константы скорости от начальной концентрации Ni2+;
![]() - зависимость степени
пересыщения (
- зависимость степени
пересыщения (![]() ) от начальной концентрации Ni2+;
) от начальной концентрации Ni2+;
![]() - зависимость индукционного
периода от начальной концентрации Ni2+.
- зависимость индукционного
периода от начальной концентрации Ni2+.
Полученное уравнение описывает процесс
химического осаждения соединений никеля в интервалах: ![]() г/л; рН=6,5-10,5;
Т=285-305 К; τ=10-150 минут.
г/л; рН=6,5-10,5;
Т=285-305 К; τ=10-150 минут.
Был проведен химический анализ осадков,
полученных при утилизации отработанных никельсодержащих растворов, состав
которых наведен в таблице.
Таблица – Состав осадков
|
Отработанный раствор |
Результаты химического
анализа, % масс. |
||||
|
Ni2+ |
Fe3+ |
СО32- |
Cl- |
SO42- |
|
|
Сульфатный высококонцентрированный раствор |
47,5 |
0,12 |
29,3 |
0,05 |
0,95 |
|
Хлоридный высококонцентрированный раствор |
45,2 |
0,19 |
22,3 |
1,2 |
0,1 |
|
Сульфатный низкоконцентрированный раствор |
47,8 |
0,05 |
23,5 |
0,01 |
0,95 |
|
Хлоридный низкоконцентрированный раствор |
45,8 |
0,03 |
23,4 |
0,1 |
0,05 |
|
Государственный стандарт 4466-78 «Никель углекислый
основной» |
42-48 |
0,02 |
Не регл. |
0,01 |
0,05 |
Сравнительный анализ осадков показал, что по
основным показателям они соответствуют действующему ГОСТу 4466-78 «Никель (II)
углекислый основной водный». Осадки могут быть использованы как добавки к шихте
при металлургическом производстве, в качестве сырья при приготовлении раствора
нитрата никеля (II) в технологии катализаторов нанесенного типа, а также в
качестве основного исходного сырья в технологии катализаторов смешанного типа
после дополнительной отмывания для снижения содержания примесей.
Литература:
1. Грищенко С.Г. Проблемы использования
техногенных отходов промышленного комплекса Украины / С.Г. Грищенко, А.В.
Ноговицын, В.Ф. Макагон // Новые, технологические и экономические аспекты
использования отходов: тезисы докл. -
Киев,
1998.- с. 3 - 5.