Д-р. хим.
наук, проф. Бельтюкова С.В., канд. хим. наук, Ливенцова Е.О., канд. хим. наук,
доц. Малинка Е.В., канд. хим. наук Теслюк О.И.
Одесская национальная академия пищевых технологий,
Украина
Твёрдофазно - люминесцентное определение
4–гидрокси–3–метоксибензальдегида
в коньяках и бренди
Изучено комплексообразование и спектрально
- люминесцентные свойства комплексных соединений ионов тербия (III) с 4–гидрокси–3–метоксибензальдегидом
(ванилином), разработана методика определения ванилина методом люминесцентной
спектроскопии в коньяках и бренди,
основанная на сенсибилизации люминесценции ионов Tb (III) в тонком
слое сорбента.
Ключевые
слова: ион тербия (III), люминесценция, тонкослойная хроматография, альдегид.
I. Введение
Ароматические
альдегиды находят широкое применение в пищевой и парфюмерной промышленности.
Так, например, ванилин используют в пищевой промышленности в качестве
ароматической добавки в кондитерские изделия и алкогольные напитки. Бензальдегид
применяют в парфюмерных композициях. В связи с этим актуальной остается
проблема определения ароматических альдегидов в самых разнообразных объектах.
Для их определения используют спектрофотометрические [1, 2], хроматографические
методы анализа [3-5] и капиллярный электрофорез [6]. Эти методы характеризуются
низкими пределами обнаружения, однако требуют наличия дорогостоящей и сложной
аппаратуры. Использование предварительного концентрирования и разделения анализируемой
системы в тонком слое сорбента на хроматографической пластинке приводит к
оптимизации аналитического сигнала, увеличению чувствительности и селективности
метода, полученные результаты разделения легко оценить визуально и
количественно.
II. Постановка
задачи
Ванилин
(Ван) – 4–гидрокси–3–метоксибензальдегид, содержится в виде гликозида в плодах
и является основным компонентом экстракта ванили. Применяется, в основном,
синтетический, в качестве ароматизатора в пищевой, парфюмерной и
фармацевтической промышленности. В малых концентрациях ванилин содержится в
таких продуктах питания, как оливковое и сливочное масло, малина. Выдержка в
дубовых бочках придаёт ванильный аромат некоторым
алкогольным напиткам. Причём, чем старше напиток, тем больше
содержание в нём ванилина [5, 6]. Содержание ванилина, например, в коньяке с возрастом до 5-ти
лет не превышает 0,46–0,56 мкг/мл, в коньяках марочных и коллекционных с
возрастом от 3-х до 20-ти лет –
колеблется от 1,3 до 6,4 мкг/мл. Таким образом, по содержанию ванилина можно
установить примерный возраст алкогольных напитков выдержанных в дубовых бочках.
Цель
работы - разработка люминесцентной методики определения ванилина в алкогольных
напитках, основанной на сенсибилизации люминесценции ионов Tb (III) в тонком
слое сорбента.
III. Результаты
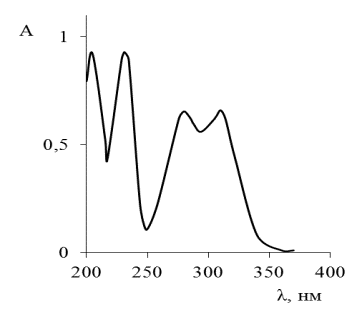
Ванилин имеет в УФ-области спектра полосы поглощения с максимумами при l = 205, 231, 280, 310 нм (рис. 1), с молярными коэффициентами поглощения 94100, 94600, 66000, 67400, соответственно. Триплетный уровень Ван, рассчитанный из спектров фосфоресценции его комплекса с Gd (III) при 77˚ К составляет 21140 см –1, что превышает энергию возбужденного состояния иона Tb (III) (20500 см–1). Поглощая энергию возбуждения, Ван передает её ионам Тb (III), которые проявляют при этом интенсивную сенсибилизированную люминесценцию в слое сорбента. В связи с этим раствор хлорида тербия (III) был использован в качестве проявляющего для обнаружения Ван на пластинках для ТСХ. В растворах люминесценция комплекса практически не обнаруживается.
Рисунок 1 - Спектр поглощения этанольного раствора ванилина СВан= 2·10–4 моль/л, l = 1 cм
Iлюм, отн. ед.
 λ, нм
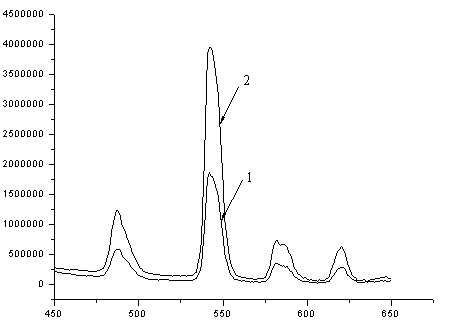
λ, нмРисунок 2 - Спектр люминесценции сорбата Tb (III) (1) и
сорбата комплекса Tb (III) с Ван (2)
(λвозб= 280нм; СTb(III)= 1·10–4 моль/л; СВан= 2·10–4 моль/л)
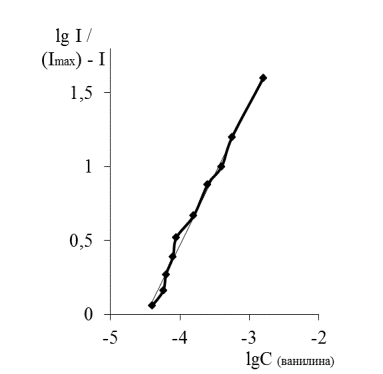
В спектрах люминесценции сорбата Tb (III) и сорбата комплекса Tb (III) с Ван (рис. 2) наблюдаются полосы, соответствующие энергетическим переходам иона Tb (III): 5D4→7F6 (487,5 нм), 5D4→7F5 (544,25 нм), 5D4→7F4 (585 нм), 5D4→7F3 (620 нм). Наиболее интенсивной является полоса, соответствующая энергетическому переходу 5D4→7F5 (544,25 нм). Увеличение интенсивности люминесценции (Iлюм) иона Tb(III) на пластинках ТСХ в присутствии Ван может свидетельствовать об образовании комплексного соединения. Интенсивность люминесценции Тb (III) на пятне хроматограммы зависит от концентрации иона лантанида в проявляющем растворе, и максимальна при концентрации Тb (III) 1·10-3 моль/л. Методом ограниченного логарифмирования определён состав комплексного соединения Tb (III) – Ван, который составил 1:2 (рис. 3).
n = 2,0
Рисунок 3 - Определение состава комплекса Tb(III) – Ван методом ограниченного логарифмирования (С Tb(III) =1·10-3 моль/ л)
С целью выбора оптимальных условий и режимов хроматографирования исследовали ряд неподвижных фаз, которые различаются своими свойствами – Silufol, Silufol –UV 254, Sorbfil, СТХ – 1А. Наилучшим оказалось применение хроматографических пластинок Silufol, на которых изображения пятен Ван было более четким и пригодным для количественного анализа.
В качестве подвижной фазы были исследованы следующие смеси растворителей: бензол: метанол: уксусная кислота (100:50:1), бензол: диоксан: уксусная кислота (90:25:4). Наиболее оптимальной оказалась система нейтрального характера, в частности, бензол: этилацетат в соотношении 70:30. Подвижность (Rf) ванилина в этих условиях составила 0,57. Исследование влияния объема пробы, наносимого на пластинку, показало, что наилучший результат достигается при нанесении пробы объемом 1 мкл. Наибольшая интенсивность люминесценции Тb (III) на пластинке обнаруживается в присутствии уротропина 40%-ного (рН 6,8–7,2). При значении рН 4,0, создаваемом с помощью ацетатного буферного раствора и при значениях рН 9,2–9,5, создаваемом с помощью ацетатно-аммиачного буферного раствора, Iлюм Тb (III) на пластинке значительно уменьшалась.
Интенсивность люминесценции сорбата комплекса Тb(III) – Ван пропорциональна концентрации Ван в широком интервале 10–6 – 10–2 моль/ л, что позволяет сделать вывод о том, что указанный сорбат комплекса может быть использован в качестве аналитической формы для определения ванилина.
Методика апробирована
на алкогольных напитках – коньяках и бренди выдержки до 5-ти лет (табл. 1). Содержание ванилина в
анализируемых образцах варьируется от 0,55 мкг/ мл
до 1,45 мкг/ мл, что согласуется с литературными данными [5, 6].
Таблица 1 - Результаты определения ванилина в коньяках
и бренди
|
№ п/п |
Марка алкогольного напитка |
Добавка, мкг/ мл |
Найдено в пробе с добавкой, мкг/ мл |
Содержание ванилина, мкг/ мл |
Sr |
|
1. |
коньяк «Болград» (Украина) |
0,5 |
1,41 |
0,91 |
0,07 |
|
1,0 |
1,93 |
0,93 |
0,08 |
||
|
2. |
бренди «Шабо» (Украина) |
0,5 |
1,27 |
0,77 |
0,06 |
|
1,0 |
1,80 |
0,80 |
0,06 |
||
|
3. |
коньяк «Таврия» (Украина) |
0,5 |
1,05 |
0,55 |
0,05 |
|
1,0 |
1,57 |
0,57 |
0,06 |
||
|
4. |
бренди «Metaxa»
(Греция) |
0,5 |
1,91 |
1,41 |
0,07 |
|
1,0 |
2,45 |
1,45 |
0,08 |
IV. Выводы
Изучено комплексообразование и спектрально
- люминесцентные характеристики комплексных соединений ионов тербия (III) с 4-гидрокси-3-метоксибензальдегидом
(ванилином), разработана методика определения ванилина методом люминесцентной
спектроскопии в коньяках и бренди,
основанная на сенсибилизации люминесценции ионов Tb (III) в тонком
слое сорбента, которая является более
простой и экспрессной.
Литература:
1. Staden J.F., Britz H.E. Flow injection spectrophotometric determination of total carbonyls in hydrocarbons by reaction with vanillin // Anal. Chim. Acta. – 1997. – V. 351. – Р. 281-289.
2. Чернова Р.К., Гусакова Н.Н., Еременко С.Н., Доронин С.Ю. Фотометрическое определение анилина и его мононитропроизводных с п- диметиламинокоричным альдегидом. // Изв. ВУЗов. Химия и хим. технология. – 1996. – Т. 39. – № 6. – С. 33 – 35. 3. Герасимов А.В., Горнова Н.В., Рудометова Н.В. Определение ванилина и этилванилина в пищевых ароматизаторах ванинольного направления методом планарной (тонкослойной) хроматографии. // Журн. аналит. хим. – 2003. – Т. 58. – № 7. – С. 758 – 766. 4. Савчук С.А.. Власов В.И., Апполонова С.А. и др. Применение хроматографии и спектрометрии для идентификации подлинности спиртных напитков // Журн. аналит. хим. – 2001. – 56, №3. – С. 246-264.5. Савчук С.А., Колесов Г.М. Хроматографические методы в контроле качества коньяков и коньячных спиртов // Журн. аналит. хим. – 2005. – 60, №8. – С. 848-868.6. Паносян А.Г., Мамиконян Г., Торосян М. и др. Определение фенольных альдегидов в коньяках и винах методом капиллярного электрофореза: новые маркеры качества коньяка // Журн. аналит. хим. – 2002. – 57, №4. – С. 422-428.