ПРЯМАЯ
КОНВЕРСИЯ ПРОПАН–БУТАНОВОЙ ФРАКЦИИ В МЕТАНОЛ
Иджагбуджи А.А., Целищев А.Б., Лория М.Г., Федотов Р.Н.
Технологический Институт СНУ имени В. Даля (г. Северодонецк).
В данной работе разработан способ синтеза
метанола из алканов с использованием динамической кавитации перекисью водорода,
который характеризуется простотой и достаточной эффективностью. Pазработка технологических основ процесса неполного
окисления пропан–бутановой
фракции (C3–C4) в метанол на основе реакций с гидроксильным радикалом и технологии,
реализующей эти процессы, которая характеризуется простой технологической схемы
и аппаратурного оформления, низкой энергоемкостью, и улучшенными
технико-экономическими и экологическими показателями. В работе [1] показано, что одним из самых эффективных
активаторов углеводородов является гидроксильный радикал. В работе [2] проведен
анализ способов получения гидроксильного радикала в промышленных условиях путем
воздействия различных физических факторов. При работе с метанолом наиболее
приемлемым является кавитационный способ получения гидроксильного радикала. В
качестве генератора гидроксильных радикалов в данном случае предлагается
процесс динамической кавитации перекиси водорода [3].
Механизм
процесса. На первом этапе перекись
водовода под действием динамической кавитации
разлагается на два радикала
•OН.
Н2O2 + кавитация → 2 •ОH (1)
При взаимодействии генерированного •OH-радикала с молекулой
алкана образуется алкильный радикал и молекула воды:
CnH2n+2 + •OН→ •CnH2n+1 + H2O
(n = 3, 4) (2)
Последующий гомолитический разрыв С–С связи
алкильного радикала с образованием алкенов и нового радикала является хорошо
известным радикально-цепным процессом в термическом крекинге. В условиях нашего
процесса селективность образования
радикалов •СН3 близка к 99
% [4]:
•CnH2n+1 → •СН3
+ Cn-1H2n-2 (n = 3, 4) (3)
Замыкает цикл реакция синтеза метанола [5].
•СН3 + •OН → СН3OН. (4)
Реактор состоит из верхней и нижней части – 1 и 2, которые соединены между собой при
помощи фланцевого соединения 3. В верхней части реактора расположен входной
патрубок 4 линии высокого давления, по которому в реактор подается смесь
алканов и раствора перекиси водорода. На форсунке 5 эта смесь дросселируется до
давления, при котором начинается процесс кавитации. Кавитированный таким
образом поток направляется на конусоподобное препятствие 6, на котором за счет
деформации потока происходит вторая волна кавитации. В верхней части реактора 1
протекают реакции гидроксильного радикала с углеводородами. Далее реакционная
смесь через сетчатую решетку 7 и диффузор 8 собирается в нижней части реактора
2. Установка
работает следующим образом. Алканы всасываются насосом высокого давления 6 и
смешивается с водным раствором перекиси водорода, который подается через
регулирующий вентиль 1 и ротаметр 2. С давлением ~ 16 МПа и расходом ~ 5
л/минуту, реакционная смесь подается в кавитационный реактор.
В случае
переработки пропан–бутановой
фракции исходный газ брался из баллона с пропан–бутановым газом и через редуктор подавался на лабораторную установку. Избыточное давление газа в сети составляло не более 0,03 МПа.
В реакторе проходят процессы по
уравнениям (1) – (4). С выхода реактора продукты реакции отводятся в
приемную емкость 8, где они отстаиваются и в последующем разделяются. В случае если степень превращения углеводородного сырья недостаточна, она может быть повторно.
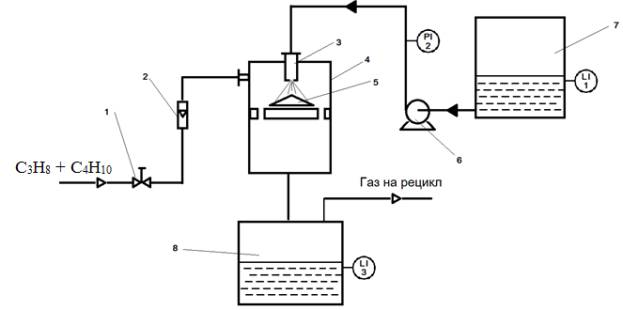
Схема лабораторной установки переработки
углеводородного сырья, которая работает по кавитационному способу: 1, 10, 11– регулирующий вентиль, 2– ротаметр, 3– форсунка,
4–кавитационный реактор, 5–конусообразное препятствие, 6–насос высокого
давления, 7, 8–емкости с раствором перекиси водорода и сырьем, 8–емкость для
продуктов реакции.
Выводы:
1. Разработана конструкция реакционного аппарата и
технологическая схема лабораторной и полупромышленной установки синтеза
метанола, которые позволили достичь ~10 % степени
конверсии пропан-бутановой
фракции в метанол за один проход при полном отсутствии побочных продуктов
реакции.
2. Впервые предложено получать метанол непосредственно из
пропан-бутановой
фракции путем динамической кавитации его с перекисью водорода. Обоснован
механизм процесса. Разработана конструкция кавитационного реактора.
Літературa:
1. Целищев А.Б. Физико-химические основы
фото-автокаталитического процесса окисления метана в метанол / А.Б. Целищев, О.И. Захарова, М.Г. Лория, И.И. Захаров // Вопр.
химии и химтехнологии. – 2009. –№. 4. –С.
43–55.
2. Целищев А.Б. Анализ физико-химических
методов получения гидроксильного радикала / А.Б.Целищев, М.Г.Лория, И.И.Захаров
// Вісник Національного технічного університету «ХПІ». – 2011. –№. 65. –С.
111–124.
3. Асеев Д.Г. Детектирование ОН радикалов
в процессе гидродинамической кавитации и в сонореакторе люминисцентными
методами / [Д.Г. Асеев, Р.М. Кенжин, В.О. Стояновский, А.А. Батоева, А.М.
Володин] // Тезисы XXIII симпозиума «Современная химическая физика» 23 Cентября – 04 Oктября 2011 г. Туапсе (Россия): Из-во МГУ, 2011. –С. 81–83.
4. Ivan I. Zakharov, Ayodeji A.
Ijagbuji, Alexei B. Tselishtev, Marina G. Loriya, Roman N. Fedotov, The new pathway for methanol synthesis: Generation of
methyl radicals from alkanes // Journal
of Environmental Chemical Engineering –№ 3 (2015) –p. 405 – 412.
5. Целищев А.Б. Кавитационный способ повышения качества моторных топлив /
А. Б. Целищев, И. И. Захаров, М. Г. Лория, П. Й. Елисеев, В. А. Носач, А. А. Иджагбуджи // Хімічна промисловість України. – 2014. –№ 2 (121). –C. 39–42.