Шайхутдинов
В.М.1, Жаппар Н.К.1, Тен О.А.1, Балпанов Д.С.1,
Еркасов Р.Ш.2, Бакибаев А.А.3
1ТОО «BioGeoTec»,
Казахстан
2Евразийский Национальный
Университет, Казахстан
3Томский
Государственный Университет, Россия
Консорциум для биовыщелачивания арсенопиритных
концентратов, устойчивый к высоким концентрациям мышьяка
Процесс биоокисления
для переработки упорных золотосодержащих руд и концентратов был внедрен в 1986
году. Технология биоокисления BIOX® была успешно применена на золотом руднике
Fairview в Южной Африке [1]. Данная технология показала высокую надежность, и в
настоящее время в мире существует 19 подобных производств [2].
Метод бактериального вскрытия
упорных золотосодержащих руд и концентратов основан на применении автотрофных
бактерий Acidothiobacillus ferrooxidans, при которых золотосодержащие сульфиды железа
окисляются до конечных химических соединений (сульфата и арсената железа,
серной кислоты) без применения высоких давлений и температур. Освобождающееся при
этом золото становится доступным для выщелачивания цианистыми растворами. Метод
бактериального выщелачивания при переработке мышьяксодержащих руд является
экологически чистой технологией, обладает также экономической эффективностью [3].
Немаловажным аспектом
при разработке технологии чанового биовыщелачивания мышьяксодержащей золотой
руды является устойчивость штаммов к повышенному содержанию мышьяка в
технологических растворах. Проведено изучение природной устойчивости штаммов S.
thermosulfidooxidans ST-12 и ОT-1 и At. ferrooxidans AF-2
к мышьяку. Для этого штаммы засевали на среды с различной концентрацией мышьяка
– 0,5 г/л, 1,0 г/л, 1,5 г/л, 2,0 г/л. Анализ активности штаммов определяли по
динамике окисления двухвалентного железа. На рисунке 1 представлено влияние ионов
мышьяка на скорость окисления железа умеренно-термофильными штаммами.
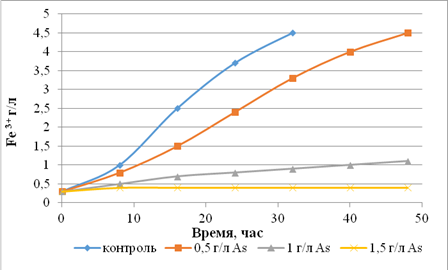
а
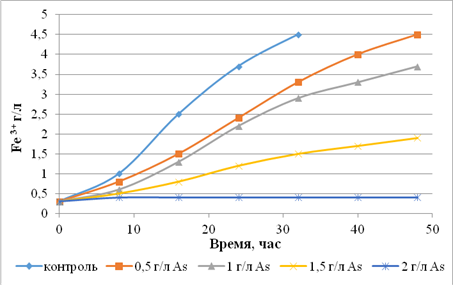
б
а – S. thermosulfidooxidans SK-4; б – S. thermosulfidooxidans
ОT-1
Рисунок 1 – Изучение
устойчивости умеренно-термофильных штаммов к ионам мышьяка
При отсутствии мышьяка
оба умеренно-термофильных штамма полностью окисляли двухвалентное железо за 30
часов роста. Внесение в среду арсената натрия в концентрации 0,5 г/л
значительно снижало окислительную активность обоих штаммов – полное окисление
двухвалентного железа произошло лишь на 48 час роста. Было замечено, что штамм S.
thermosulfidooxidans ОT-1 обладает большей природной устойчивостью к
мышьяку по сравнению со штаммом S. thermosulfidooxidans SK-4
– внесение в среду арсената натрия в концентрации 1 г/л и 1,5 г/л почти
полностью ингибировало окислительную способность штамма S. thermosulfidooxidans SK-4,
в то время как штамм S. thermosulfidooxidans ОT-1 сохранял окислительную
активность на уровне 60% и 30% соответственно. На рисунке 2 представлено
влияние ионов мышьяка на скорость окисления железа At. ferrooxidans AF-2.
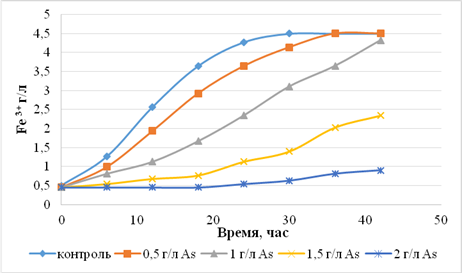
Рисунок 2 – Изучение устойчивости At. ferrooxidans AF-2 к ионам мышьяка
При отсутствии токсических веществ At. ferrooxidans AF-2 полностью окислял двухвалентное железо за 30 часов роста.
При внесении в среду ионов мышьяка в концентрации 1,0 г/л полное окисление
двухвалентного железа наблюдалось лишь на 36 час роста, при внесении 1,5 г/л –
на 42 час роста.
В дальнейшем была
проведена направленная селекция на увеличение устойчивости штаммов к высокому
содержанию мышьяка. Направленную селекцию осуществляли путем последовательных
пересевов на питательные среды, в которых постепенно увеличивали содержание
мышьяка. Динамика окисления железа адаптированными бактериями представлена на
рисунке 3.
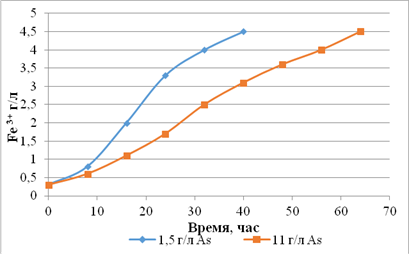
а
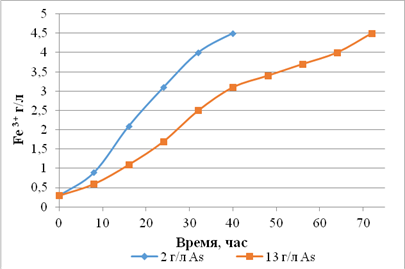
б
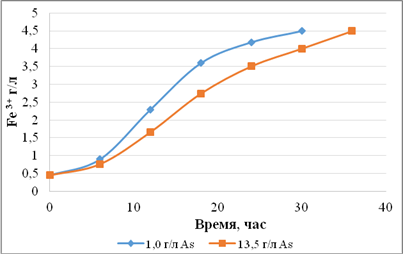
в
а
– штамм S. thermosulfidooxidans SK-4; б – штамм S.
thermosulfidooxidans ОT-1;
в
– Acidithiobacillus
ferrooxidans AF-2
Рисунок
3 – Динамика окисления железа адаптированными штаммами
В результате
проведенной селекции у штамма S.thermosulfidooxidans
SK-4 устойчивость
к мышьяку была увеличена с 0,5 г/л до 11 г/л, у штамма S.thermosulfidooxidans
ОT-1 с 1 г/л до 13 г/л, у At. ferrooxidans AF-2 с 1,0
г/л до 13,5 г/л, что соответствует необходимым технологическим требованиям для обработки
арсенопиритных золотых руд и концентратов.
В
технологии бактериального выщелачивания основная роль железоокисляющих
микроорганизмов заключается в регенерации ионов трехвалентного железа, которые
являются главным окислителем сульфидных минералов. Окисление минералов ионами
железа сопровождается образованием на поверхности слоя элементарной серы, что
приводит к экранированию дальнейшего действия окислителя. В связи с этим важно
применение микроорганизмов как железоокисляющей активностью так и с сероокисляющей
активностью.
На основе
адаптированных к высоким содержаниям мышьяка штаммов составлен консорциум
хемолитотрофных бактерий, состоящий из железоокисляющего штамма At. ferrooxidans AF-2, умеренно-термофильных штаммов S.thermosulfidooxidans
SK-4 и ОT-1 с железо и сероокисляющей
активностью.
Литература
1 Kaksonena A. H.,
Mudunurua B. M., Hackl R. The role of microorganisms in gold processing and
recovery-A review // Hydrometallurgy. – 2014. – Vol. 142. – P. 70-83.
2
Brierley, J.A. Present and future commercial applications of biohydrometallurgy
// Hydrometallurgy. – 2001. – Vol. 59. – P. 233-239.
3
Bhalerao S.A. Bioleaching: An Economic Alternative for the Mining Industry: A
Review // International journal of biotechnology and biosciences. – 2011. –
Vol. 1. – P. 67-72.