В. О. Саліонов
Запорізький державний медичний університет
СИНТЕЗ НОВИХ ПОХІДНИХ 1,2,4-ТРІАЗОЛ-3-ТІОЛІВ, ЯКІ МІСТЯТЬ ТІОФЕНОВИЙ ЦИКЛ
Вступ. Відомо, що похідні
1,2,4-тріазол-3-тіолів досить широко застосовуються у фармацевтичній, медичній,
ветеринарній практиках або у народному господарстві [1, 2, 3, 6]. Аналіз наукової літератури показав, що
перспективним шляхом у створенні нових біологічно активних речовин є синтез
іліденгідразидів 4-R-5-R1-1,2,4-тріазол-3-ілтіо ацетатних кислот. Сполуки цього класу
застосовуються як високоефективні антиоксидантні, протимікробні або
протигрибкові засоби, і крім того знаходять застосування в синтетичній
та аналітичній хімії [4, 5].
Тому, ми вважали за доцільне синтезувати ряд іліденгідразидів
2-((3-(тіофен-2-іл)-1H-1,2,4-тріазол-5-іл)тіо)ацетатних кислот та встановити
фізико-хімічні властивості отриманих сполук.
Матеріали і методи
дослідження. Хімічні
назви сполук наведено згідно номенклатури IUPAC (1979 рік) і рекомендацій IUPAC
(1993 рік). Дослідження фізико-хімічних властивостей отриманих сполук проводили
згідно методів, які наведені у Державній Фармакопеї України.
Синтез іліденгідразидів
2-((3-(тіофен-2-іл)-1H-1,2,4-тріазол-5-іл)тіо)ацетатної кислоти (сполуки 5-6,
табл.1). До 0,01
моль відповідного гідразиду (сполука 1) додають 10 мл метанолу, 0,2 мл
концентрованої HCl і нагрівають до розчинення, додають 0,01 моль відповідного альдегіду
(5-нітрофуральдегід, 3-(5-нітрофуран-2-іл)акрилальдегід). Суміш залишають при
кімнатній температурі на 15 год, осад відфільтровують, промивають диетиловим
естером і висушують. Отримані іліденгідразиди являють собою коричневого
(сполуки 5, 6) кольору речовини, важко розчинні у воді і органічних
розчинниках. Для аналізу сполуки очищені із ацетатної кислоти.
Синтез іліденгідразидів
2-((4-(метил-, етил-,
феніл-)-5-(тіофен-2-іл)-4H-1,2,4-тріазол-3-іл)тіо)ацетатних кислот (сполуки
7-14, табл.1). До
0,01 моль відповідного гідразиду (сполуки 2-4) додають 10 мл метанолу, 0,2 мл
концентрованої HCl і нагрівають до розчинення, додають 0,01 моль відповідного альдегіду
(2- і 3-нітробензальдегід, 5-нітрофуральдегід,
3-(5-нітрофуран-2-іл)акрилальдегід). Суміш залишають при кімнатній температурі
на 15 год, осад відфільтровують, промивають диетиловим естером і висушують.
Отримані іліденгідразиди являють собою жовтого (7, 10, 13), коричневого (9, 11,
12, 14) та світло-коричневого (8) кольору речовини, важко розчинні у воді і
органічних розчинниках. Для аналізу сполуки (7-9, 11, 13-14) очищені із
ацетатної кислоти, сполуки 10 та 12 перекристалізовано з метанолу.
Результати та їх обговорення. Іліденгідразиди 2-((4-R-5-(тіофен-2-іл)-4H-1,2,4-тріазол-3-іл)тіо)ацетатних
кислот (сполуки 5-14, табл.1) були отримані шляхом взаємодії відповідних
гідразидів 2-((4-R-5-(тіофен-2-іл)-4H-1,2,4-тріазол-3-іл)тіо)ацетатних
кислот (сполуки 1-4) з 2- і
3-нітробензальдегідом, 5-нітрофуральдегідом,
3-(5-нітрофуран-2-іл)акрилальдегідом в середовищі метилового спирту при наявності
каталітичної кількості концентрованої HCl (схема. 1).
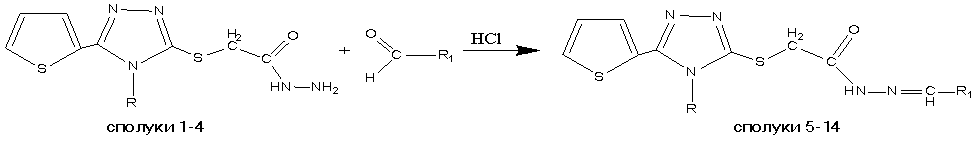 R
= Н, CH3, C2H5, C6H5; R1 = Ar, Het;
R
= Н, CH3, C2H5, C6H5; R1 = Ar, Het;
Схема
1. Синтез
іліденгідразидів 2-((4-R-5-(тіофен-2-іл)-4H-1,2,4-тріазол-3-іл)тіо)ацетатних
кислот
Фізико-хімічні константи отриманих сполук наведені в таблиці 1. У всіх випадках будова синтезованих
сполук підтверджена комплексним використанням елементного аналізу (табл. 1),
ПМР- (табл. 2) та ІЧ- спектроскопії.
Таблиця 1
Фізико-хімічні
константи іліденгідразидів 2-((4-R-5-(тіофен-2-іл)-4H-1,2,4-тріазол-3-іл)тіо)ацетатних
кислот
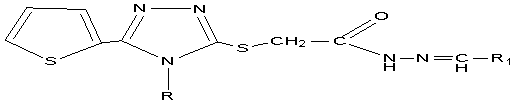
|
Cполука |
R |
R1 |
Т пл., оС |
Брутто-формула |
Вихід, % |
|
5 |
Н |
|
133-135 |
C13H10N6O4S2 |
79 |
|
6 |
Н |
|
143-145 |
C15H12N6O4S2 |
73 |
|
7 |
CH3 |
|
155-157 |
C16H14N6O3S2 |
90 |
|
8 |
CH3 |
|
228-230 |
C14H12N6O4S2 |
88 |
|
9 |
CH3 |
|
213-215 |
C16H14N6O4S2 |
83 |
|
10 |
C2H5 |
|
185-187 |
С17Н16N6O3S2 |
77 |
|
11 |
C2H5 |
|
170-172 |
С15Н14N6O4S2 |
90 |
|
12 |
C2H5 |
|
210-212 |
С17Н16N6O4S2 |
93 |
|
13 |
C6H5 |
|
221-223 |
С19Н14N6O4S2 |
89 |
|
14 |
C6H5 |
|
200-202 |
С21Н16N6O4S2 |
89 |
Продовж. табл. 1
|
Сполука |
Знайдено, % |
Обчислено, % |
||||||
|
C |
H |
N |
S |
C |
H |
N |
S |
|
|
5 |
41,38 |
2,64 |
22,17 |
16,89 |
41,26 |
2,66 |
22,21 |
16,95 |
|
6 |
44,68 |
2,98 |
20,75 |
15,88 |
44,55 |
2,99 |
20,78 |
15,86 |
|
7 |
47,82 |
3,50 |
20,87 |
15,91 |
47,75 |
3,51 |
20,88 |
15,93 |
|
8 |
43,01 |
3,07 |
21,38 |
16,30 |
42,85 |
3,08 |
21,42 |
16,34 |
|
9 |
45,99 |
3,38 |
20,01 |
15,25 |
45,92 |
3,37 |
20,08 |
15,33 |
|
10 |
49,12 |
3,88 |
20,13 |
15,36 |
49,03 |
3,87 |
20,18 |
15,40 |
|
11 |
44,39 |
3,48 |
20,65 |
15,74 |
44,33 |
3,47 |
20,68 |
15,78 |
|
12 |
47,16 |
3,74 |
19,48 |
14,79 |
47,21 |
3,73 |
19,43 |
14,83 |
|
13 |
50,29 |
3,09 |
18,54 |
14,08 |
50,21 |
3,10 |
18,49 |
14,11 |
|
14 |
52,41 |
3,37 |
17,55 |
13,32 |
52,49 |
3,36 |
17,49 |
13,35 |
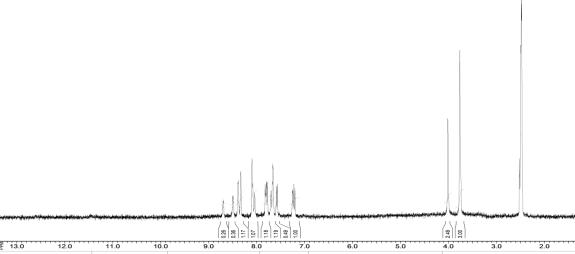
Рис. 1. 1Н-ЯМР-спектр
2-((4-метил-5-(тіофен-2-іл)-4H-1,2,4-тріазол-3-іл)тіо)-N'-(3-нітробензиліден)ацетогідразиду
(сполука 7)
Аналізуючи результати спектральних досліджень слід зазначити, що в 1Н
ЯМР спектрі 2-((4-метил-5-(тіофен-2-іл)-4H-1,2,4-тріазол-3-іл)тіо)-N'-(3-нітробензиліден)ацетогідразиду
(рис. 1) наявні сигнали протонів метилового радикалу, зв’язаного з ядром
1,2,4-тріазолу при 3,78 м.ч. (3Н) у вигляді синглету, метиленової групи
зв’язаної з атомом Сульфуру, яка проявляється у вигляді синглету при 4,01 м.ч.
(2Н), сигнали протонів тіофенового кільця, які реєструються у вигляді триплету
7.22 м.ч. (1Н) та 2-х дублетів при 7,58 м.ч. (1H) та при 7,69 м.ч. (1H). Крім того, спостерігаються сигнали
протонів ароматичного кільця у вигляді триплету при 7.80 м.ч. (1Н), двох
дублетів при 8.07 м.ч. (1Н) та при 8.35
м.ч. (1Н), синглету при 8.70 м.ч. (1Н), а також сигнали метинової групи, яка
фіксується у вигляді синглету при 8,49 м.ч. (1H).
Таблиця 2
1H-ЯМР - спектри синтезованих сполук
|
Сполука |
1H ЯМР (DMSO-d6 δ ppm) |
|
5 |
7.81 (d, 1H,
thiophene), 7.75 (d, 1H, thiophene), 7.69 (d, 1H, furan), 7.53 (s, 1H, CH),
7.45 (d, 1H, CH), 7.23 (t, 1H, thiophene), 7.18 (s, 1H, NH), 7.12 (d, 1H,
furan), 4.01 (s, 2H, CH2). |
|
6 |
7.78 (d, 1H,
thiophene), 7.71 (d, 1H, thiophene), 7.66 (d, 1H, furan), 7.56 (s, 1H, CH),
7.44 (d, 1H, CH) 7.38 (t, 1H, CH), 7.18 (t, 1H, thiophene), 6.81 (s, 1H, NH), 6.73 (d, 1H, furan), 4.01 (s, 2H, CH2). |
|
7 |
8.70 (s, 1H, Ar),
8.49 (s, 1H, CH), 8.35 (d, 1H, Ar), 8.07 (d, 1H, Ar), 7.80 (t, 1H, Ar), 7.69
(d, 1H, thiophene), 7.58 (d, 1H, thiophene), 7.22 (t, 1H, thiophene), 4.01 (s, 2H, CH2), 3.78 (s, 3H, CH3). |
|
8 |
7.68 (d, 1H, thiophene), 7.58 (d, 1H, furan, 1H,
thiophene), 7.52 (s, 1H, CH), 7.21 (t, 1H, thiophene), 7.04 (s, 1H, NH), 6.93 (d, 1H, furan), 4.01 (s, 2H, CH2), 3.62 (s, 3H, CH3). |
|
9 |
7.97 (d, 1H,
thiophene), 7.72 (m, 1H, furan, 1H, thiophene), 7.61 (d, 1H, CH), 7.16 (t,
1H, thiophene), 7.02 (d, 1H, CH, 1H, NH), 6.92 (d, 1H, furan), 6.85 (s, 1H, CH), 3.98
(s, 2H, CH2), 3.76 (s, 3H,
CH3). |
|
10 |
8.61 (s, 1H, CH),
8.15 (d, 1H, Ar), 8.11 (d, 1H, Ar), 8.03 (m, 2H, Ar, NH), 7.81 (d, 1H,
thiophene), 7.77 (m, 1H, Ar, 1H, thiophene), 7.26 (t, 1H, thiophene), 4.21
(m, 2H, CH2), 3.99 (s, 2H, CH2), 1.33 (t, 3H, CH3). |
|
11 |
7.68 (d, 1H, thiophene), 7.58 (d, 1H, furan, 1H,
thiophene), 7.51 (s, 1H, CH), 7.22 (t, 1H, thiophene), 7.04 (s, 1H, NH), 6.93
(d, 1H, furan), 4.25 (m, 2H, CH2),
4.00 (s, 2H, CH2),
1.30 (t, 3H, CH3). |
|
12 |
7.93 (d, 1H, thiophene), 7.71 (d, 1H, furan, 1H,
thiophene), 7.36 (s, 1H, CH), 7.26 (t, 1H, thiophene), 7.17 (d, 1H, furan),
7.11 (s, 1H, CH), 7.07 (s, 1H, CH), 7.01 (s, 1H, NH), 4.11 (m, 2H, CH2),
3.99 (s, 2H, CH2), 1.29 (t, 3H, CH3). |
|
13 |
7.97 (d, 1H, thiophene), 7.81 (d, 1H, thiophene),
7.68 (m, 2H, Ar, 1H, furan), 7.57 (m, 3H, Ar, 1H, CH), 7.27 (t, 1H,
thiophene), 7.11 (d, 1H, furan), 7.01
(s, 1H, NH), 4.04 (s, 2H, CH2). |
|
14 |
7.99 (d, 1H, thiophene), 7.81 (d, 1H, furan, 1H,
thiophene), 7.66 (m, 2H, Ar), 7.54 (m, 3H, Ar), 7.46 (s, 1H, CH), 7.29 (t,
1H, thiophene), 7.04 (s, 1H, NH), 7.01 (s, 1H, CH), 6.94 (d, 1H, furan), 6.92
(s, 1H, CH), 4.04 (s, 2H, CH2). |
Висновки
1.
Взаємодією
відповідних гідразидів 2-((4-R-5-(тіофен-2-іл)-4H-1,2,4-тріазол-3-іл)тіо)ацетатних кислот з 2- і 3-нітробензальдегідом, 5-нітрофуральдегідом,
3-(5-нітрофуран-2-іл)акрилальдегідом в середовищі метилового спирту при
наявності каталітичної кількості концентрованої HCl отримано 10 нових сполук.
2.
За
допомогою елементного аналізу, ПМР- та ІЧ- спектроскопії підтверджено будову
синтезованих сполук, а їх індивідуальність доведено хроматографічно.
Література:
1. Кныш Е. Г. Синтез, физико-химические
и биологические свойства N- и S‑замещенных 1,2,4-триазола : дис. … д-ра фармац. наук / Кныш
Е. Г. – Х., 1987.– 350 с.
2. Панасенко О. І. Синтез, перетворення,
фізико-хімічні та біологічні властивості аміно- і тіопохідних 1,2,4-тріазолу :
дис. … д-ра фармац. наук / Панасенко О. І. – К., 2005. – 396 с.
3. Парченко В. В. Синтез, перетворення,
фізико-хімічні та біологічні властивості в ряді 5-фурилзаміщених
1,2,4-тріазол-3-тіонів: Дис. д-ра
фармац. наук. – Запоріжжя, 2014. – 683 с.
4. Парченко В. В., Панасенко А. И., Кныш
Е. Г. / Синтез, физико-химические и
биологические свойства новых илиденгидразидов
2-[5-(фуран-2-ил,2-метилфуран-3-ил)-4R-1,2,4-триазол-3-илтио]ацетатных кислот
// Вестник новых медицинских технологий.
– 2013. – т. 20. – №. 3.
5. Самелюк Ю. Г., Каплаушенко А. Г.
Синтез та фізико-хімічні дослідження гідразидів та іліденгідразидів
2-(5-(4-метоксифеніл),(3, 4, 5-триметоксифеніл)-1, 2, 4-триазол-3-ілтіо)
ацетатних кислот //Фармацевтичний журнал. – 2013. – №. 4. – С. 66-71.
6. Щербина Р. О. Аналіз фармакологічної
активності похідних 1,2,4-тріазолу / Р. О. Щербина // Фармацевтичний часопис. –
2014. – № 4. – С. 145–150.