Д.т.н. Бегун П.И.
Санкт-Петербургский государственный электротехнический
университет «ЛЭТИ» им. В.И. Ульянова (Ленина) (СПбГЭТУ «ЛЭТИ»)
МОДЕЛИРОВАНИЕ ПРОЦЕССА
ГИПЕРТРОФИИ СКЕЛЕТНЫХ МЫШЦ
Гипертрофия
скелетных мышц представляет собой процесс их долговременной адаптации к
физическим нагрузкам. В ответ на физическую нагрузку и в зависимости от ее
характера, в организме человека выделяют два вида гипертрофии –
саркоплазматическую и миофибриллярную. Саркоплазматическая гипертрофия мышц
представляет собой увеличение объема мышечных волокон за счет увеличения объема
их саркоплазмы. При миофибриллярной гипертрофии мышц увеличение объема мышечных
волокон происходит за счет увеличения количества и объема миофибрилл.
Саркоплазматическая гипертрофия мышц – адаптация организма к выносливости, а
миофибриллярная – к силовым нагрузкам.
Нагрузки на структуры организма относительно
низкой интенсивности, но большой длительности, приводят к увеличению количества
митохондрий в волокнах, вовлеченных в соответствующий вид деятельности. Вокруг
этих волокон возрастает число капилляров. Повышается выносливость - способность к длительной мышечной активности
при минимальном утомлении. Изменения происходят не только в скелетных мышцах,
но и в дыхательной и сердечно - сосудистой системах. К мышцам поступает больше
кислорода.
Растягивание мышц за пределы их нормальной длины приводит к развитию
другого типа гипертрофии - добавляются новые саркомеры. В литературе [1 - 5] рассмотрены различные гипотезы, объясняющие
процессы, происходящие в мышцах, и приводящие к миофибриллярной гипертрофии
мышечных волокон. В [6], представленные в публикациях, гипотезы
классифицированы, как: 1)”энергетическая”,
2)”ацидозная”, 3)”гипоксийная”,
4)”механическая”.
По первой
гипотезе гипертрофия мышечных волокон наступает при нарушении равновесия между
потреблением и восстановлением аденозинтрифосфата. По второй - при закислении
внуренней среды организма, связанном с накоплением в тканях кислых продуктов
обмена веществ. По третьей – при кислородном голодании тканей, обусловленном
ограниченным поступлением крови в сдавленные капилляры и артериолы
сокращающихся мышц. По четвертой – при механическом
повреждение мышечных волокон, за которым следует их регенерация.
Четвертая гипотеза получила в настоящее время широкое распространение. К сожалению, представленные и обсуждаемые в публикациях модели процессов передачи усилия от миофиламентов к сухожилию (представляющих одну из интереснейших проблем мышечного сокращения) не отражают адекватно современное представление о функционировании мышцы.
Современные геометрические модели мышечного волокна и скелетной мышцы, приведенные в [1 - 6] включают: 1)
соединительно – тканные структуры: перемизий, эндомизий, эпимизий; 2) базальную мембрану, которая коллагеновыми волокнами
связана с эндомизием; 3) сарколемму, которая, прикрепленными к
ней костамерами, фиксирует периферические миофибриллы,
по линиям Z –дисков находящихся
на границах саркомеров, 4) гибкие элементы цитоскелета - цитоскелетные и промежуточные
филаменты, фиксирующие миофибриллы; 5) сетчатую
структуру Z –дисков.
На рис. 1 приведена, предлагаемая автором, схема сокращенного
мышечного волокна, при сокращении мышцы
в концентрическом режиме (рс, рв, - давление
соответственно в сарколемме и волокне).
Сарколемма связана с сухожилием.
При сокращении саркомеров уменьшается продольный размер сарколеммы, стягиваемой
костамерами, соединенными с Z –дисками. Несжимаемая внутритканиевая жидкость, перемещаясь, создает
давление и расширяет сарколемму. Деформированная сарколемма перемещает
внутритканиевую жидкость и деформирует базальную мембрану и эндомизий. Деформация
мышечных волокон вызывает последовательно деформацию перемизиума и эпимизиума. При
этом внутритканиевая жидкость, находящаяся в промежутках между соединительно – тканными структурами, перемещаясь
создает давления и деформирует их. Деформированные соединительно – тканные
структуры уравновешивают нагрузку, которую преодолевает мышца.
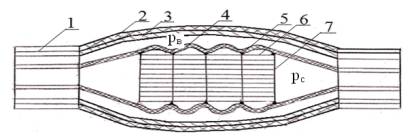
Рис. 1. Схема деформированного мышечного волокна: 1
–сухожилие, 2 - эндомизиум, 3- базилярная мембрана, 4 сарколемма, 5 – костамеры,
6,7 - продольные и поперечные филаменты (волокна) цитоскелета
При концентрическом и эксцентрическом режимах
расширению сарколеммы препятствуют поперечные элементы цитоскелета, связывающие
миофибриллы. Они разрушаются, если
напряжения, возникающие в них, превышают допускаемые. При их разрушении нарушается
ориентация миофибрилл. Повреждаются Z-диски, сарколемма, а также
саркоплазматический ретикулум, содержащий кальций. Повреждение сарколеммы
приводит к активации клеток - сателлитов. За этим следует их деление и
последующая гипертрофия мышечного волокна. Повреждение Z-дисков и саркоплазматического
ретикулума приводит к выделению ионов кальция в сарколемму. Ионы кальция
активируют специальные ферменты – протеазы, разрушающие сократительные белки и
элементы цитоскелета. Проникновение в
мышечные волокна лейкоцитов вызывает мышечные боли.
При
эксцентрическом режиме к изгибным деформациям соединительно – тканных структур
добавляются деформации растяжения. Расширенная сарколемма вытягивается. Вытягиваются
продольные волокна – филаменты цитоскелета. Если напряжения, возникающие в них,
превышают допускаемые и эти волокна разрушаются. Дезориентация миофибрилл возрастает. Это
объясняет большие повреждения мышечных волокон при силовой тренировке в эксцентрическом
режиме по сравнению с концентрическим [3].
Испытывая
неизбежные сокращения, в уже нарушенном цитоскелете, саркомеры приводят к еще
большему разрушению матричной структуры внутри сарколеммы. Это объясняет,
отмеченное во многих исследованиях, явление мышечного дискомфорта и боли в
мышцах, достигающих максимума через 24 – 48 часов после силовых упражнений. Вначале боль локализуется в проксимальных и
дистальных отделах мышцы (местах концентрации напряжений), затем
распространяется на всю мышцу. Множество исследований демонстрировало,
что эксцентрические сокращения приводят к увеличению уровня креатинкиназы в
течение 24 – 48 часов после упражнения и может сохраняться в течение 3–6 дней.
Креатинкиназа - внутримышечный фермент, ответственный за то, чтобы поддержать
адекватные уровни ATФ в течение мышечного
сокращения. Его появление в крови интерпретируется как увеличенная
проницаемость или разрушение мембраны мышечного волокна [2].
При
силовых нагрузках постоянно происходят повреждения и регенерация мышц.
Адаптация к новым нагрузкам - процесс,
протекающий через разрушение структур и последующую регенерацию.
Приведенная модель позволяет представить последовательность процессов,
происходящих в мышце при концентрическом и эксцентрическом режимах сокращения.
После разрушения цитоскелета начинается процесс ремоделирования мышцы.
Увеличивается синтез сократительных белков. Миофиламенты реконструируются в
соответствии с величиной новых внешних воздействий. Увеличивается площадь
поперечного сечения всех типов волокон.
Литература
1. Proske U., Morgan D. L. Muscle damage
from eccentric exercise: mechanism, mechanical signs, adaptation and clinical
applications //Journal of Physiology,2001.–
V. 537.– N2, P. 333 –
345
2.
Friden J., Lieber R.L. Eccentric
exercise-induced injuries to contractile and cytoskeletal muscle fibre
components //Acta Physiol. Scand. 2001, 171, P. 321 - 326
3.
Gibala M.J., MacDougall J.D., M.A.Tarnopolsky M.A., W.T.Stauber W.T. ,
Elorriaga A. Changes in human skeletal muscle ultrastructure and force
production after acute resistance exercise //J.Appl. Physiology, 1995.– V.
78.-N.2.– P. 702 - 708
4.
МacDougall
J. D. Hypertrophy and Hyperplasia // The Encyclopedia of
Medicine. Strength and Power in Sport / Ed. P. V. Komi.
Bodmin; Cornwall: Blac Publishing. 2003. V. 3. P. 252 - 264
5.
Вайн А. А. Явление передачи механического напряжения в скелетной
мышце. Тарту: Изд. Тартуского университета, 1990. 34 с.
6. Самсонова А.В. Гипертрофия
скелетных мышц человека; Учеб. пособие. - 3-е изд. — СПб.: Политехника, 2015. —
159 с.