Д.х.н., профессор Баешов А.Б., к.т.н. Айболова Г.Т.,
к.х.н. Тулешова Э.Ж.
Институт органического катализа и электролхимии им.
Д.Сокольского, Казахстан
Международный казахско – турецкий университет им. Ясави,
Казахстан
РАЗРАБОТКА ТЕХНОЛОГИЧЕСКОЙ ОСНОВЫ ПОЛУЧЕНИЯ
НИТРАТА КАЛИЯ АНОДНЫМ ОКИСЛЕНИЕМ ОКСИДА
АЗОТА (ІІ) НА ЖЕЛЕЗНЫХ КУСКОВЫХ
ЭЛЕКТРОДАХ
В настоящее время
переработка газов, содержащие в составе оксид азота (ІІ) в целях
обезвреживания, связано с разработкой методов получения из него полезных
веществ.
Техника очищения
газов, в связи с видами аппаратов, фильтрующие пыли и вредные газы очень
разнообразны. Известны механические
(из твердых частиц и очистка жидких каплей), сорбические и химические методы
(каталитическое оксиление, термическое разложение и др.). обезвреживания газов
и получение из него полезных соединений Эффективные методы обезвреживания
газов, содержащие оксид азота (ІІ) до сих пор не известны. Несмотря на то, что
предлагаются множество методов и данных по переаработке оксида азота (ІІ), до
сих пор этот вопрос остается
актуальной.
При разработке
технологий получения экологически чистого и безотходной продукции, при
обезвреживании газов, содержащих соединения оксида азота (ІІ), также при
получении элементного азота и
соединений азота огромное значение имеют электрохимические методы.
Интерес у
электрохимиков вызывает определение возможностей участия мелких газообразных
пен, как и порошковые вещества в электродных реакциях.
Результаты литературного
обзора дают понять, что процессы электрохимического окисления оксида азота (ІІ)
очень мало исследованы.
В последнее время
при проведении электрохимических процессов вместо плоских электродов считается
лучше использовать кусковые, порошковые, суспензионные электроды, так как они
не допускают пассивацию электрода, повышают скорость прохождения процесса.
Рассмотрено, что эти электроды вполне возможно использовать в целях окисления
газовых пен. В нашей работе
обезвреживание путем окисления оксида азота (ІІ) в щелочной среде
использовали мелкие кусковые электроды (диаметром 1.5 мм, длиной 3.0 мм). Эти
электроды отличаются высокой поверхностной площадью.
Электролиз
проводили в гальваностатистических условиях, в 3 М растворе гидроксида калия,
электролизере объемом 100 мл. Газы оксида азота пропускали с нижней части
анодного пространства электролизера с определенной скоростью. В основных
экспериментах объем газа пропускающие на электролизер – 300 мл. Скорость
газовой струи регулировалось с помощью трехгорлого крана. Во всех условиях
электролиз проводили 0,5 часов [2-4].
Как показали
результаты предыдущих экспериментов, при
пропускании исследуемого газа с помощью компактного плоского электрода через щелочной раствор, наблюдается окисление
оксида азота (ІІ) до нитрат-иона. Выход
по току не превысило 3,1%.
На электроде
происходит окисление оксида азота (ІІ):
![]() E0 = + 1,049 B (1)
E0 = + 1,049 B (1)
Оқсид азота
(ІІ) может окисляться с атомарным кислородом, выделющийся на аноде:
NO + O →NO2 (2)
Образовавшийся газ
оксида азота (ІІ) растворяясь в щелочи
образует нитрат- и нитрит-ионы:
2NO2 + 2KOH → KNO3
+ KNO2 + H2O (3)
При растворении оксида азота (ІІ) в щелочи,
превышается стехиометрическая доза кислорода и образуют только нитрат-ионы:
4NO2
+ 4KOH + O2 → 4KNO3 + 2H2O (4)
Исследованы
влияния плотности тока кускового электрода, концентрации электролита, толщина
слоя кускового электрода, объем газа на степень окисления и на выход по току
окисления оксида азота (ІІ). Электролиз проводили при комнатной температуре.
После электролиза
сделаны анализы на количество нитрат-ионов образовавшихся в растворе.
При
оптимальных условиях (i = 100 A/м2, [KOH] = 3,0 – 5,0M, d=2см, V=300мл) степень окисления оксида азота составляет 97 %, выход по току окисления - 66,6 – 85,2 %.
Опираясь на
результаты исследования можно предложить принципиально технологическую схему обезвреживания
оксида азота (ІІ) на кусковых электродах, являющийся отходом производства цветной
металлургии и другие. На 1 рисунке видно, пыли
цветных металлов в плавильной печи фильтруются в электрофильтровальном
аппарате, а оксид азота (ІІ) проходит этапы адсорбции (в целях выделения из
дымчатых газов) и дессорбции, затем собираются на газгольдере и отправляются на электролиз.
Электролиз
проводится соединенную в цепочку или в нескольких электролизерах, в 3М растворе гидроксида калия. Электродное пронстранство
разделено катионитовой мембраной МК-40. В качестве катода использовали железную
пластинку, а в качестве анода кусковые железные электроды. При поляризации
оксид азота (ІІ) окисляется на аноде, а оставшийся газ направляется в анодное
пространство электролизера. Образовавшийся нитрат калия, выпаривают,
кристализуют, сушат, а затем отправляют потребителю.
Если
вместо гидроксида калия использовать гидроксид натрия то можно получить нитрат
натрия.
По результатам
проведенной работы видно, что максимальная степень окисления и выход по току оксида
азота (ІІ) наблюдается в 3М растворе гидроксида калия, плотность тока электрода
100 А/м2, толщина кускового слоя δ = 2 см.
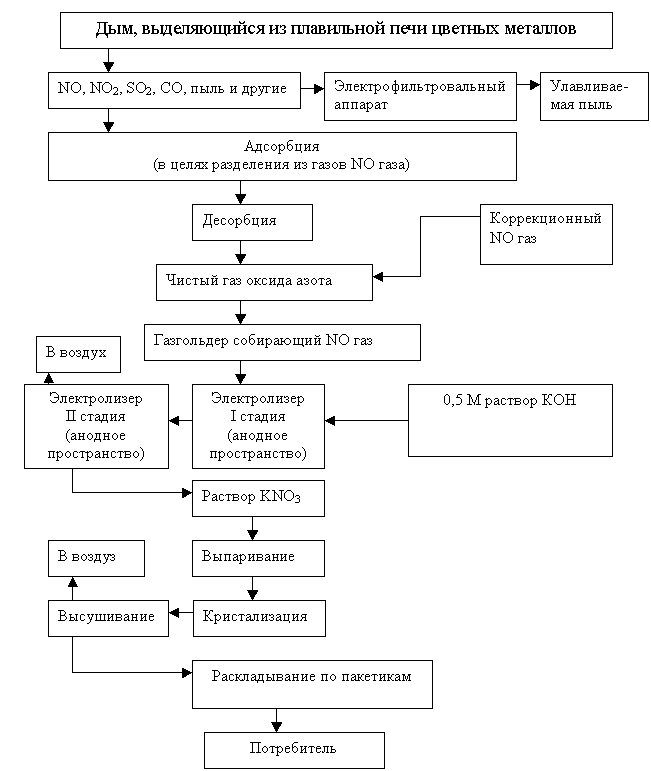

Рисунок 1. Принципиально технологическая схема
получения нитрата калия
Таким образом,
установлено, что в щелочной среде при окислении оксида азота (ІІ) образуется
нитрат калия. С помощью этого метода можно обезвредить отходы заводов цветной
металлургии и получать из них соединения азота.
Литература:
1. Кипарисов С.С. Использование порошкообразных псевдоожиженных электродов
для получения цветных металлов. ЦНИИ цветмет МЦМ. СССР, серия Производство
тяжелых и цветных металлов. – М., 1981, вып 9. -148 с.
2. Шваб Н.А., Каздобин К.А., Агужен А.Я. Электроосаждение
металлов подгруппы меди на псевдоожиженые электроды из электродных
материалов. Цветные металлы, 1985, №5,
с.35-37.
3. Интенсификация электрохимических процессов. Сборник научных
трудов. Отв. ред. проф. Томилов А.П. – М., Наука, 1988. -213 с.
4. Айболова Г.Қ., Баешов А.Б.
Азот (ІІ) оксидін электрохимиялық жолмен сілтілі ортада тотықтыру
// Промышленность Казахстана. – Алматы, 2005. №5. - С. 93-94.
5.
Предпатент 18716 РК. Способ окисления оксида азот (ІІ)/ Баешов А.Б., Айболова
Г.К., Баешова А.К. опубл. 15.08.2007, Бюл. № 8.