д.х.н., профессор
Буркеев
М.Ж., д.х.н., профессор Тажбаев Е.М., Жаппар Н.К., доктор PhD Жапарова Л.Ж.,
к.х.н., доцент Жумагалиева Т.С., Борсынбаев А.С., Ержан К.
Карагандинский
государственный университет им. Е.А. Букетова
Республика Казахстан
Полимолочная кислота – как полимерный носитель противотуберкулезного
препарата «Изониазид»
Целенаправленная доставка
лекарства является одной из наиболее важных задач фармакологических
исследований. Особенно это очевидно в отношении противоопухолевых и
противотуберкулезных химиотерапевтических средств, так как длительное лечение
сильнодействующими препаратами в большинстве случаев приводит к проявлению
множественной лекарственной устойчивости, сопровождающейся выраженными
побочными эффектами [1]. Связыванием лекарств, применяемых в терапии рака и
туберкулеза, с полимерной матрицей, можно добиться увеличения терапевтической
эффективности препаратов. При этом выбор полимерной основы, используемых в
качестве носителей лекарств, во многом определяется составом и строением
биологически активного вещества. Одним из природных
полимеров, используемых для транспорта лекарственных препаратов является поли(D,L)-молочная)
кислота и ее сополимеры с гликолевой кислотой [2]. В качестве лекарства
использовали широко применяемый в терапии туберкулеза препарат - изониазид. Наличие
в молекулах полимера и лекарственного вещества соответствующих связей,
гидроксильных, карбоксильных и аминных групп, а также гетероатомов,
способствует образованию водородных, донорно-акцепторных, диполь-дипольных
взаимодействий и позволяет получить новые лекарственные формы в виде наночастиц
[3].
В данной работе изучена
возможность связывания противотуберкулезного препарата «Изониазид» с поли(D,L)-молочной
кислотой с целью повышения эффективности и уменьшения терапевтической дозы
лекарства.
Экспериментальная часть
Материалы. 80 %-ный раствор молочной кислоты (![]() = 1,185
г/см3), толуол, хлорид олова (II), диоксан,
поливиниловый спирт, хлороформ, этанол.
= 1,185
г/см3), толуол, хлорид олова (II), диоксан,
поливиниловый спирт, хлороформ, этанол.
Методика
получения полимолочной кислоты
Синтез полимолочной кислоты
прямой поликонденсацией молочной кислоты проводили в толуоле [4]. В
круглодонную трехгорлую колбу, снабженную насадкой Дина-Старка, обратным
холодильником и термометром загружали 80 %-ный раствор молочной кислоты для
удаления присутствующей воды. Далее загружали хлорид олова (II) в качестве катализатора и осуществляли
поликонденсацию при температуре 120-130°С продолжительностью 12 часов.
Полученный вязкий, светло-желтый продукт сушили, после перекристаллизации
которого выделяли светло-бежевый порошок.
Молекулярная масса образца полимолочной кислоты составила 710.
Другим способом получения
высокомолекулярного полилактида является полимеризация с использованием в
качестве исходного сырья лактида [5].
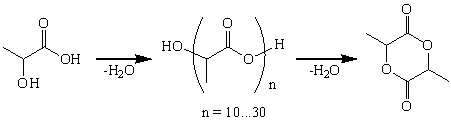
Получение лактида заключается в перегонке
молочной кислоты, сначала под атмосферным давлением, при нагреве смеси до
температуры 110–125°С. При этом вода легко отгоняется, до получения
90–95 %-го раствора молочной кислоты. Затем дальнейшая отгонка растворной
воды затруднена, поэтому для ее удаления применяли вакуум. Процесс протекает в
две стадии: на первой стадии при дегидратации молочной кислоты образуется
линейный олиголактид, на второй стадии олигомер деполимеризуется и при
пониженном давлении образует лактид. Далее в приемнике конденсировался
светло-желтый продукт.
Полученный лактид перекристаллизовывали из
этилацетата и получали белые кристаллы с температурой плавления 94,5°С, сушили
в вакууме при 30°С в течение 4 часов, чтобы удалить
следы воды. Данный лактид в дальнейшем использовали в качестве исходного
продукта при получении полимолочной кислоты.
На третьей стадии осуществляли полимеризацию
лактида в присутствии хлорида
олова (II), при температуре 150–170°С в течение 3–6 ч.:
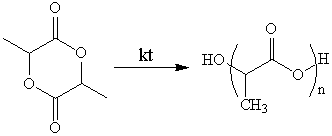
После проведения
полимеризации продукт
растворяли в хлороформе, переосаждали в этаноле,
затем твердый остаток промывали несколько раз в этаноле для удаления непрореагировавших реагентов.
Очищенный полимер собирали и сушили
в вакуумном шкафу при 50°С в течение 6 часов до постоянной массы.
Характеристика наночастиц полимолочной кислоты
Фотонная корреляционная спектроскопия
Размер частиц и
полидисперсность наночастиц, а также молекулярную массу полимера определяли
методом фотонной корреляционной спектроскопии на приборе Malvern Zetasizer Nano S90 (Malvern
Instruments Ltd., Malvern, UK) при температуре 250С
и при значении угла рассеивания 900.
ИК- и 1Н ЯМР спектроскопии
Образцы ПМК были
приготовлены с KBr для метода инфракрасной спектроскопии. ИК-спектры сделаны на
Инфракрасном Фурье-спектрометре «ФСМ-1201» от 450 см-1 до 4000 см-1
при разрешении 2 см-1 и 1 сканирований.
ЯМР 1Н-спектры
регистрировали на спектрофотометре «AVANCE AV
300» фирмы «Bruker» при рабочей частоте 300 МГц и температуре 25°С. В качестве внутреннего
стандарта использовали гексаметилдисилоксан.
Определение степени связывания изониазида
кондуктометрическим методом
Степень связывания изониазида с полимолочной кислотой определяли
кондуктометрическим методом. Электропроводность растворов измеряли на приборе
Conductivity meter Type OK-102 (Hungary) №1182 и ООО «Эконикс-Эксперт», ИНН/КПП
7728209000/772801001 (Москва). При этом использовали платиновые электроды;
термостат марки UTU-2/77 (Polanol) и термостатируемую ячейку (293 К) объемом 25
мл.
Для построения калибровочной кривой предварительно
в мерной колбе объемом 100 мл готовили растворы изониазида различных
концентраций: 0,0125; 0,025; 0,05;
0,1; 0,2 %
и фиксировали электропроводность. Данные для построения калибровочного графика
приведены в таблице 1.
Таблица
1. Данные для построения калибровочного графика гидразида изоникотиновой кислоты по электропроводности
|
№п/п |
С («Изониазида»),
мкг/мл |
χпракт, ·10-4,
См/см |
|
1 |
0,0125 |
2,1 |
|
2 |
0,025 |
3,9 |
|
3 |
0,05 |
6,5 |
|
4 |
0,1 |
12 |
|
5 |
0,2 |
24,73 |
По градуировочному графику определяли концентрацию
несвязавшегося лекарства. Поскольку электропроводность растворов является
величиной аддитивной, определили электропроводности компонентов системы и
сделали соответствующие поправки.
Степень связывания препарата рассчитывали по разности исходного и
несвязавшегося изониазида. Для концентраций лекарства 0,0125-0,2 % изменение
значений удельной электропроводности подчиняется линейному уравнению у=120,8х+0,398.
Корреляционные коэффициенты равнялись 0,9983.
Определение выхода наночастиц
гравиметрическим методом
Взвешивали пустые алюминиевые тигли на весах с точностью 1*10-4 мг,
наполняли каждый тигель 0,05 мл раствором наночастиц и выпаривали в сушильном
шкафу в течении 2-х часов при температуре
800С, затем снова взвешивали тигли.
Результаты и их обсуждение
Полимолочную кислоту
получали по описанной выше методике, полученный продукт представляет собой белый
порошок без запаха, молекулярная масса которого составила 1500. ИК и ЯМР 1Н-спектры
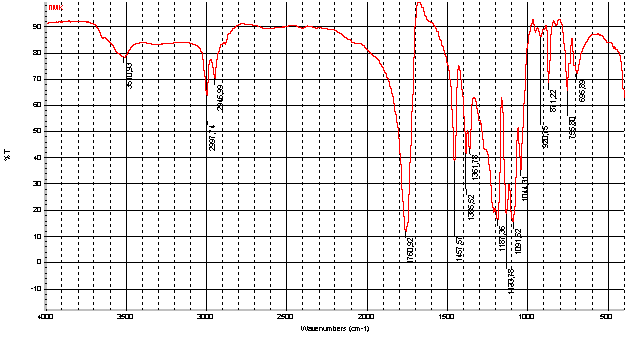
образцов показаны на рисунке 1 (а) и (б) соответственно.
(а)
(б)
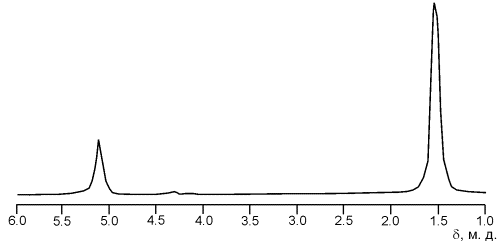
Рисунок 1 - ИК- (а) и ЯМР 1Н-спектры
(б) полимолочной кислоты
Как видно из рисунка, на ИК спектре
(рис. 1 (а)) присутствуют
характеристические полосы поглощения в области 1758~1763
см-1 и 2994~ 2997 см-1, относящиеся к колебаниям связей C=O и –CH2,
пик поглощения при 1184~1190см-1
для C-O-C эфирной группы
свидетельствует о формировании –СОО-. Также присутствуют полосы поглощения
в 1452~1457см-1 и
1382~1389 см-1, соответствующая колебаниям
связи –CH(CH3) и все эти пики указывают, на
образование полимолочной кислоты. Типичные колебания –CH связи на кольце лактида
резонирует в характерной области 932~934 см-1 не
наблюдались во всех образцах, что указывает на раскрытие кольцевого цикла
лактида. ЯМР 1Н-спектр (рис. 1
(б)) полимолочной кислоты доказывает, что реакция успешна прошла,
наблюдаются интенсивные сигналы протонов СН3 и СН групп в области
1,52 и 5,13 м. д. соответственно.
Активностью в отношении вируса туберкулеза обладает
значительное число препаратов, одним из них является фармакологический препарат
«Изониазид» (I).
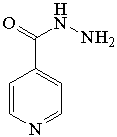
(I)
Затем
проводили иммобилизацию полимера лекарством по нижеследующей методике: в стакане, содержащем
5 мл диоксана, растворяли рассчитанное количество полимолочной кислоты и обрабатывали
ультразвуком. В отдельном стакане растворяли лекарство в воде и добавляли
поливиниловый спирт, затем смешивали содержимое обоих стаканов и перемешивали
на магнитной мешалке в течение 2-х
часов.
Физико-химические
характеристики наночастиц полимолочной кислоты, содержащих лекарство, определяли методом фотонной
корреляционной спектроскопии: результаты по полидисперсности полимерных
наночастиц приведены на рисунке 2.
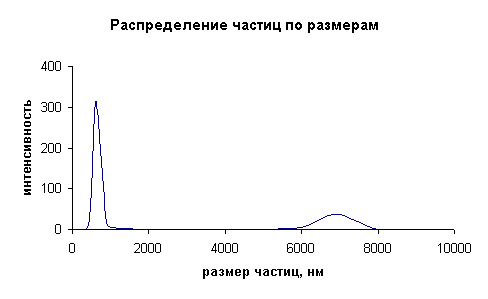
Рисунок 2. Распределение
наночастиц полимолочной кислоты, иммобилизованных изониазидом
Из
рисунка видно, что в системе имеются две группы частиц: средний размер первой
группы частиц составляет 600 нм, а вторая группа частиц имеет коагуляционный
характер и их размер превышает 6000 нм, поэтому эти агломераты отделяли от
частиц нанометрического размера трехкраткным центрифугированием при 14 500
об/мин. Выделенные частицы, размерами 850 нм с полидисперсностью 0,106, диспергировали
в воду обработкой ультразвуком в течение 10 минут, после чего размер наночастиц
составил 270 нм.
Полученные
полимерные наночастицы, иммобилизованные
изониазидом, сушили до постоянной массы. Выход полимерных наночастиц, содержащих лекарство, составил 82,5%. Затем полимолочную кислоту, содержащую
изониазид, растворяли в рассчитанном количестве хлороформа и несвязавшееся лекарство
экстрагировали бидистиллированной водой, и определяли степень
связывания. Степень связывания, определенная кондуктометрическим методом, составила
48 %, что является высоким показателем и указывает на перспективность
применения таких систем для доставки противотуберкулезного препарата «Изониазид».
Таким образом, нами показана возможность получения
наночастиц полимолочной кислоты, иммобилизованных противотуберкулезным
препаратом «Изониазид».
Литература:
1.
Soppimath S.K., Aminabhavi M. T., Kulkarni R.
A., et al. Biodegradable
polymeric nanoparticles as drug delivery devices. Review // J. Controlled
Release. – 2001. – Vol. 70. – P. 1-20.
2.
Батырбеков Е.О.,
Мошкевич С.А., Жубанов Б.А. и др. Современное состояние и перспективы в области
поиска новых противотуберкулезных препаратов.// Алматы,
– 1998. – C. 48.
3. Машковский М.Д. Лекарственные средства. // Пособие для
врачей.// М.: Медицина // Ч.2. – 1972. – Т. 1. – С. 580.
4. Фомин В. А., Коровин Л.П. и др. Исследование процесса получения молочной кислоты – основного
полимера биоразлагаемых пластиков // Пластмассы. – 2009.
– № 12. – С. 11-17
5.
Jalaber M.,
Fraschini C., Prud’Homme R. E. et al. Synthesis
and characterization of poly(L-lactide)s and poly(D-lactide)s of controlled
molecular weight. // Journal of
Polymer Science // Part A, – 2007. – Vol. 45. №.
10. – P. 1944–1955.