Химия и химическая технология/ 5.Фундаментальные основы создания новых материалов и технологий
Янкин А.М., Федорова О.М., Упоров
С.А., Ведмидь Л.Б.
Институт металлургии УрО РАН,
Екатеринбург, Россия
Влияние
содержания кислорода на резистивные свойства NdSr2Mn2O7±d
Манганиты редкоземельных элементов c перовскитоподобной кристаллической структурой вызывают интерес исследователей из-за
уникальных физических свойств, в частности, колоссального магнитосопротивления
(КМС), проявляющегося вблизи точки Кюри. К их числу относятся и фазы
Раддлесдена-Поппера (Р-П), построенные по блочному принципу из
взаимопроникающих фрагментов структур перовскита и каменной соли. При изучении
физических свойств в Sr2-x La1+xMn2O7 [1] выяснено, что баланс между антиферромагнетизмом и
ферромагнетизмом в этих составах очень
чувствителен к степени окисления марганца. В [2] отмечается, что электронные
свойства Ln2-xSr1+xMn2O7 определяются размерами лантаноидов и степенью
окисления марганца. Окисление марганца в этих работах контролировалось
изменением катионного состава (соотношения разнозарядных ионов Ln и Sr), но не было
попыток осуществлять такой контроль,
меняя содержание кислорода в структуре (кислородную нестехиометрию
δ). Принято считать, что электрофизические свойства оксидов формируются
через создание цепочек Mn 4+ -O-Mn 3+.
Удаление атома кислорода из такой
цепочки не только изменит маршрут
перемещения носителей, но и соотношение Mn4+ /Mn3+ для
выполнения условия электронейтральности кристалла, что приведёт к
изменениям свойств.
Соединение NdSr2Mn2O7+δ отличается от других фаз Р-П тем, что
проявляет эффект КМС в широком температурном диапазоне. В этом соединении этот эффект не связан с полным
ферромагнитным упорядочением, что
позволяет регулировать физические свойства, меняя химический состав [3].
Изучению влияния кислородной нестехиометрии на резистивные свойства фазы NdSr2Mn2O7+δ
посвящена данная работа.
Экспериментальная часть
Синтез образцов. Исходные компоненты Nd2O3 марки НдО-Е, SrСO3 квалификации
ос.ч. и Mn2O3 с чистотой ³ 98%, взятые в эквимолярных соотношениях,
перемешивались в планетарной мельнице FRITSCH в
среде этилового спирта, затем смеси прессовались в таблетки диаметром 10 мм и
толщиной 1 мм и обжигались при температуре 14000С в печи Nabertherm с точностью поддержания температуры ±2о в течение 96 часов. На первом этапе
синтеза использовался один способ охлаждения – охлаждение с печью. На втором
этапе синтеза часть образцов повторно
нагревалась, выдерживалась при температуре 14000С в течение 24 часов
и закалялась в жидкий азот, ещё одна
часть закалялась на воздухе на медной пластине. В результате, в образцах,
закалённых в азот, фиксировалось содержание кислорода, которое они имели в
условиях синтеза (образец №1). В образцах, охлаждённых на воздухе, содержание
кислорода увеличилось (образец №2). В образцах, охлаждённых с печью, в
условиях, близких к равновесным, содержание кислорода становилось максимальным,
по сравнению с другими (образец №3). При подготовке образцов к измерениям
таблетки измельчались, и состав
образцов по кислороду в пределах каждой партии усреднялся.
Рентгенофазовый анализ полученных веществ выполнен с помощью
дифрактометра XRD-7000 фирмы Шимадзу, CuKa-излучение, Ni
фильтр, в диапазоне углов 20-70 по 2Q с шагом 0,03 и выдержкой на каждой точке 2 сек. В
качестве внешнего стандарта использовался чистый кремний.
Определение абсолютной кислородной
нестехиометрии образцов проводилось гравиметрическим методом при восстановлении
образцов водородом до простых устойчивых оксидов по реакции:
NdSr2Mn2O7+δ+(1,5+δ)H2=(1/2)Nd2O3+(2)SrO+2MnO +(1,5+δ)H2O (1)
При этом были сделаны допущения, что убыль массы после
восстановления водородом относится только к удалённому кислороду, а твёрдые
продукты восстановления кислородной нестехиометрией не обладают. Следует
сказать, что в [1] была сделана попытка
использовать термогравиметрическое
восстановление в токе чистого водорода для определения кислородной
нестехиометрии этих же веществ, но полностью восстановить образцы им не
удалось. В наших же экспериментах газ-восстановитель циркулировал через
ловушку, помещённую в жидкий азот для вымораживания образующихся паров воды,
что позволяло достичь очень низких значений парциального давления кислорода.
Образцы для измерений электропроводности
были подготовлены методом холодного прессования в форме дисков толщиной ~ 3 мм
и шириной ~ 12 мм при давлении 10 атм, далее производился отжиг при температуре
t=1400оС в течение 96 час. Затем для каждой
серии спеченных таблеток проводилась соответствующая термическая обработка:
закалка в азот, закалка на воздух и медленное охлаждение с печью.
Измерение электропроводности были
выполнены стандартным четырехзондовым методом на постоянном токе при его
величине I=1 mA. Образцы помещались в специальный держатель,
выполненный из фторопласта с установленными электрическими медными контактами.
Устройство помещалось в криостат RTI, температура
в котором контролировалась в автоматическом режиме в диапазоне от точки кипения
азота T=77.4 K до 273 K терморегулятором tSTAT 310 X. Для измерения
температуры использовалась термопара константан-медь. Постоянный электрический
ток на образце задавался с помощью прецизионного источника тока Б5-49 со
стабильностью 0.05 %. Измерение падения напряжения на образце производилось с
помощью вольтметра APPA-305 с точностью не хуже 0.06
%. Используемая аппаратура позволяла определять значения сопротивления в
диапазоне от 10-5 до 104 Ом. Воспроизводимость полученных результатов от опыта к опыту составляла около 5%.
Полученные результаты
Данные
рентгенофазового анализа образцов, охлажденных разными способами, приведены в
таблице 1.
Таблица
1
Параметры элементарной ячейки образцов NdSr2Mn2O7±d
|
№ образца |
Режимы охлаждения |
Параметры элементарной
ячейки |
||
|
а, нм |
с, нм |
Объем |
||
|
1 |
Закаленный в жидкий азот |
0,3842(1) |
2,0029(7) |
0,2956 |
|
2 |
Закаленный на воздухе |
0,3855(1) |
2,0095(10) |
0,2986 |
|
3 |
Охлажденный с печью |
0,3854(1) |
2,0083(10) |
0,2983 |
Из таблицы 1 видно, что увеличение скорости охлаждения
уменьшает величину параметра с, параметр а изменяется в меньшей
степени.
Величины кислородной
нестехиометрии (δ), полученные гравиметрическими измерениями после
восстановления образцов в водороде до устойчивых оксидов, а также рассчитанные
из них значения валентности марганца приведены в таблице 2. В этой же таблице
приведены значения ширины запрещенной зоны для каждого из образцов.
Таблица 2.
Величины кислородной нестехиометрии (δ) и ширина
запрещенной зоны (Eg) для образцов NdSr2Mn2O7±d.
|
№ образ-ца |
Способ охлаждения |
δ |
Расчётная валентность марганца |
Eg, meV |
|
№1 |
Закалка в азот |
-0,18 |
3,32 |
98 |
|
№2 |
Охлаждение на воздухе |
-0,09 |
3,41 |
77 |
|
№3 |
Охлаждение с печью |
0,22 |
3,72 |
60 |
Температурные логарифмические зависимости удельного
электросопротивления для образцов NdSr2Mn2O7, полученных в различных режимах, приведены на рисунке
1, где нижняя кривая – медленное охлаждение с печью (обр.№3), средняя – закалка
на воздух (обр.№2) , верхняя - закалка в азот (обр.№1).
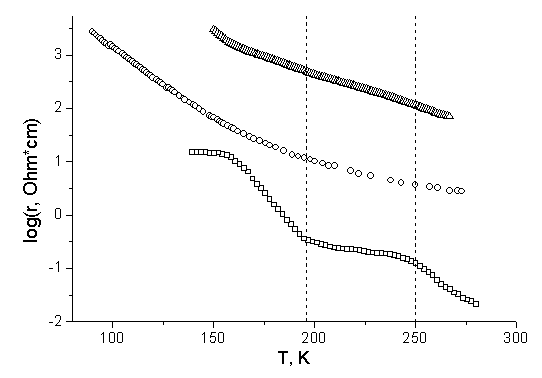
Рис.1. Зависимость логарифма электросопротивления от
температуры для образцов NdSr2Mn2O7, охлажденных с различной скоростью.
Для образцов № 1 и 2 в изученном диапазоне
температур не зафиксированы особенности на кривых log(r)-T. В случае синтеза методом медленного охлаждения
(образец № 3) на температурной зависимости электропроводности были выявлены
аномалии свойства вблизи 260 K, 210 K и 160 K. Первое
значение, скорее всего, соответствует точке Нееля для этого образца, а две
другие температуры соответствуют различным типам магнитных фазовых переходах в
подрешетках марганца и неодима.
Обнаружено, что в зависимости от
технологии синтеза электропроводность меняется радикально, при комнатной
температуре значения составляют 0.03; 2.8 и 68 Ом*см для образцов № 1, 2, 3,
соответственно. Столь сильные изменения свойства, очевидно, связаны с различной
концентрацией кислорода в каждом типе образцов. Известно, что даже небольшие
девиации по концентрации кислорода приводят к нарушению перколяционных цепочек O-Mn-O-Mn-O, по которым собственно и обеспечивается проводимость
в этих системах. Кроме того, в зависимости от кислородной стехиометрии должна
изменяется концентрация носителей заряда и электронная структура соединений.
Одной из наиболее информативных характеристик для анализа протекающих в
изученных системах изменений, в данном случае, является ширина запрещенной зоны
Eg. На полученных экспериментальных зависимостях log(r) -T-1
существует область температур, где в первом приближении, имеется
полупроводниковый характер (190-250 K), на
рис. указано вертикальными линиями. Из известного соотношения log(r)=log(r0)+Eg/2kT были
определены значения Eg, результат представлен в
таблице 1. Сопоставление литературных данных авторов [4] с нашими результатами
указывают существенное разногласие. Однако стоит отметить, что в их работе не
указаны детали режима синтеза образцов и не проведен анализ на кислородную
стехиометрию.
Рассчитанные значения величины Eg указывают на существенные изменения в электронной
структуре в зависимости от способа синтеза. Изменения Eg, вероятно, связаны не только с отклонениями в химическом
составе по кислороду, но и с дополнительными искажениями, дефектами в
кристаллической структуре, возникающими в ходе быстрой закалки. Последнее, в
свою очередь, должно отражаться на характере кристаллического поля и
соответственно на всей электронной структуре вещества.
Заключение
Полученные результаты свидетельствуют, что способ
синтеза, определяющий кислородную нестехиометрию оксида, играет ключевую роль в
формировании электронной структуры и определяет транспортные свойства изученных
материалов. Таким образом, появляется
возможность контролировать и прогнозировать служебные свойства оксидных
материалов окислительно-восстановительными отжигами в контролируемой по
кислороду атмосфере.
Работа выполнена при финансовой поддержке
РФФИ, проект № 12-03-00042а на оборудовании ЦКП «Урал-М».
Литература
1.
Battle P.D., Cox D.E., Green M.A., Millburn J.E., Spring L.E., Radaelli
P.G., Rosseinsky M.J., Vente J.F.
Antiferromagnetism, ferromagnetism, and phase separation in the GMR system Sr2-xLa1+xMn2O7
// Chem. Mater. 1997, V.9, P.1042-1049.
2. Battle P.D., Green
M.A., Laskey N., Scott K.N., Millburn J.E., Spring
L.E., Sullivan S.P., Rosseinsky M.J., Vente
J.F. Control of electronic properties by lanthanide size and
manganese oxidation state in the MnIII/MnIV Ruddlesden – Popper phases Ln2-xSr1+xMn2O7
// J.Chem. Mater. 1997. V.7(6). P. 977-988.
3. Battle P.D.,
Blundell S.J., Green M.A., Hayes W.,
Honold M., Klebe A.K., Laskey N.,
Millburn J.E., Murphy L., Rosseinsky M.J., Samarin N.A., Singleton J.,
Sluchanko N.E., Sullivan S.P., Vente J.F. Colossal magnetoresistance in Sr2-xNd1+xMn2O7
(x=0.0, 0.1) // J.Phys: Condens. Mater.
1996, V.8. L427-434.
4. Zhang J., Wang
F.,.Zhang P., Sun X., Yan Qi. Magnetic and electric properties of layered
perovskites Nd2-2xSr1+2xMn2O7 (x=0.3-0.5)
// J.Magn. Mater. 1998, V.190. P.166-170.