Химия и химические технологии/6. Органическая химия
К.х.н.
Поляков А.И., Алиева Т.А., Бедрина Е.Н., Якунина Н.Г.,
Пугачева Р.Б., к.б.н. Апрышко Г.Н.
Российский
онкологический научный центр им. Н.Н. Блохина РАМН, НИИ ЭДиТО,
г. Москва, Россия
Синтез новых функционально замещенных
пирролобензодиазепинов
1,4-Бензодиазепины (БД),
благодаря высокому терапевтическому индексу, низкой токсичности и разнообразной
биологической активности, нашли широкое применение в медицине. В последние годы
[1, 2] значительно возрос интерес к группе этого класса соединений – природным
антибиотикам в ряду пирроло-[2,1-с][1,4]-бензодиазепинов (ПБД), обладающих
противоопухолевой активностью.
В данной работе продолжены
начатые ранее исследования в области синтеза новых БД [3, 4].
С целью выявления наиболее
перспективных функционально замещенных ПБД (ФЗПБД) с потенциальной
противоопухолевой активностью для 500 виртуальных соединений оценили
вероятность проявления фармакологических эффектов, их клеточных и молекулярных
механизмов, токсических свойств с помощью компьютерной системы прогнозирования
спектра биологической активности веществ по их химической структуре PASS,
версия 11.12.01 [5, 6]. По данным прогноза для синтеза отобраны ряд
виртуальных соединений, для которых с высокой вероятностью прогнозируется
противоопухолевая активность, опосредованная проапоптотическим действием,
взаимодействием с ДНК, ингибированием протеинкиназ, при низкой вероятности
токсического действия.
Осуществлен
синтез ФЗПБД N-(5,11-диоксо-2,3,5,10,11,11a-гексагидро-1H-пирроло[2,1-c][1,4]бензодиазепин-7-ил)карбодиимин
(I), 7-изотиоциан-2,3-дигидро-1H-пирроло[2,1-c][1,4]бензодиазепин-5,11(10H,11aH)-дион
(II) и 7‑изоциано-2,3-дигидро-1H-пирроло[2,1-c][1,4]бензодиазепин-5,11(10H,11aH)-дион
(III), пригодных для использования в дальнейших
исследованиях в качестве перспективных синтонов, по принятым для этих
соединений методам [7, 8].
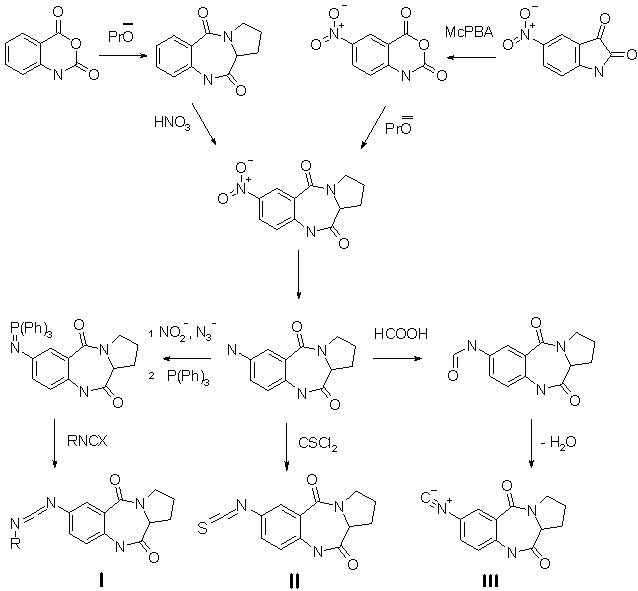
Где R =
CH3; С6Н5; cyclo-С6Н11;
X = O; S
Схема
синтеза синтонов I , II и III
Строение синтезированных соединений
доказано данными ИК, ЯМР Ή и масс-спектров.
Литература:
1. Antonow D.,
Thurston D.E. Chem. Rev., 2011, v.III (4), 2815.
2. Kamal A., Azceza S.
Mini-Reviews in Med. Chem., 2010, №10, 405.
3.
Борисов Р.С., Поляков А.И., Медведева Л.А.,
Гуранова Н.И., Воскрессенский Л.Г. Изв. АН, сер. хим., 2012, №8, 1592.
4. Borisov R.S,
Polyakov A.I., Medvedeva L.A., Khrustalev V.N., Guranova
N.I., Voskressensky L.G. Organic letters, 2010, v.12, 3894.
5.
Филимонов Д.А., Поройков
В.В. Российский химический журнал, 2006, т.50, №2, 66–75.
6. Filimonov D.A.,
Zakharov A.V., Lagunin A.A., Poroikov V.V. SAR and QSAR in Environmental
Research, 2009, v.20, №7, 679–709.
7. Ulrich H.
Chemistry and Technology of carbodiimides, Wiley, Chichester, UK, 2007, 312 p.
8.
Ugi I. Isonitrile chemistry, Acad. Press, NY., 1971, 278 p.