Химия и химические технологии/5.
Фундаментальные проблемы создания новых материалов и
технологий.
К.т.н. Налетов В.А., д.т.н. Глебов М.Б., д.т.н.
Налетов А.Ю.
Российский
химико-технологический университет им. Д.И. Менделеева,
г. Москва,
Российская Федерация, E-mail: energo@muctr.ru,
Оптимальная организация процесса паровой конверсии газа газификации на
основе информационного подхода
В соответствии со
стратегией информационного подхода к организации химико-технологических систем
(ХТС) [1,2] процесс поиска оптимального решения осуществляется в соответствии со
следующим алгоритмом:
- во-первых, поиск оптимальных весовых
коэффициентов или вкладов процессов в решение информационной задачи ХТС, исходя
из условия максимума критерия
макроуровня – макроэнтропии, которые определяют средние термодинамические
уровни процессов;
- во-вторых,
поиск для заданных оптимальных средних термодинамических уровней процессов
оптимальных условий проведения целевого превращения вещества или подстройка
целевого превращения под данные прогноза верхнего уровня. Рассмотрим решение
задачи второго уровня.
Поиск
оптимальных условий превращения вещества будем осуществлять на основании
следующей системы уравнений (для случая адиабатического реактора без отвода
теплоты):
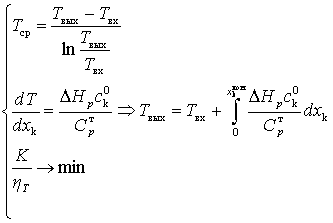 (1)
(1)
При этом
![]() ,
, 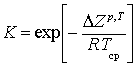 , (2)
, (2)
где ΔSр, ΔS0 – изменение термодинамической энтропии для
реального и идеального процессов, ![]() – изменение термодинамического потенциала
Гиббса в процессе, Тср –
средний температурный уровень.
– изменение термодинамического потенциала
Гиббса в процессе, Тср –
средний температурный уровень.
Первое
уравнение системы (1) представляет собой ограничение по средней температуре
процесса, второе уравнение – изменение температуры для адиабатического
реактора, третье – условие минимизации стоимости единицы информации при
постоянном значении весового
коэффициента целевого процесса.
Здесь ![]() – средняя мольная
теплоемкость смеси веществ при заданной температуре; Tнач,
Tкон – начальная и
конечная температура реактора,
– средняя мольная
теплоемкость смеси веществ при заданной температуре; Tнач,
Tкон – начальная и
конечная температура реактора, ![]() – тепловой эффект
реакции,
– тепловой эффект
реакции, ![]() – начальная
концентрация ключевого компонента;
– начальная
концентрация ключевого компонента; ![]() – степень
превращения ключевого компонента,
– степень
превращения ключевого компонента, ![]() – конечная степень
превращения ключевого компонента.
– конечная степень
превращения ключевого компонента.
Рассмотрим
процесс паровой каталитической конверсии синтез-газа, полученного при
газификации бурого угля, для обеспечения требуемого объемного соотношения Н2:СО,
равного 2:1. Реакция конверсии – экзотермическая:
![]()
В расчетах были приняты следующие исходные
данные.
Синтез-газ
после отделения газификации, очистки от пыли и кислых газов имел следующий состав:
СО
– 1082,7 м3 Н2
– 498,7 м3 СО2
– 81,23 м3
N2
– 98,78 м3 Н2О
– 71,0 м3
Массовый расход синтез-газа принят равным 1625
кг/ч. Степень превращения,
обеспечивающая требуемое соотношение Н2:CO, равна 0,5131.
Расчет равновесия реакции конверсии
определяется константой равновесия реакции Kp
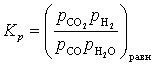 (3)
(3)
где pi (равн) –
равновесные парциальные давления компонентов.
Температурная зависимость константы
равновесия имеет следующий вид:
![]() (4)
(4)
Кинетика адиабатического реактора
определяется уравнением:
![]() (5)
(5)
Расчет скорости обратимой реакции конверсии
оксида углерода r(p,T) производился по формуле [3]:
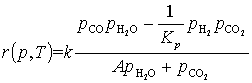 (6)
(6)
Коэффициент
A рассчитывается по уравнению:
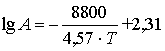 (7)
(7)
Константа скорости
рассчитывалась по уравнению:
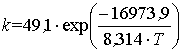 (8)
(8)
На
диаграмме рис.1 представлены результаты расчета системы уравнений (1) для
различных мольных соотношений пар: газ – m. По сути, эту диаграмму можно считать номограммой для выбора параметров
оптимального реактора, отвечающих минимуму критерия ![]() .
.
При этом в качестве
варьируемых параметров выбираются начальная и конечная температуры (Tнач , Tкон), определяющие средний температурный уровень
превращения и мольное соотношение пар:газ – m.
Как видно из
диаграммы на рис. 1, заданной степени превращения (0,5131) в пределах
определенного интервала значений температур соответствуют высокие значения
мольного соотношения пар:газ (больше
2,6).
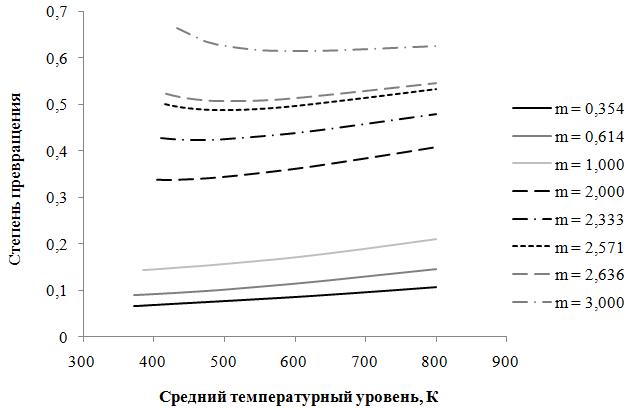
Рис.1
Зависимость степени превращения
при различных мольных соотношениях пар:газ–m и средних температурных уровнях процесса,
соответствующие минимуму критерия ![]()
Характер зависимостей
степени превращения для больших мольных соотношений пар:газ согласуется с
литературными данными, указывающими, с одной стороны, что высокая степень
конверсии (до 90%) может достигаться при достаточно высоких температурах
450-500 °С и больших мольных соотношениях пар:газ=3:1, а с другой, что, что
высокая степень превращения оксида углерода может достигаться и при низких
температурах, ввиду повышения равновесной степени превращения с понижением
температуры процесса.
На рис. 2
представлены данные для выбора оптимального мольного соотношения пар:газ с
позиции выбранного критерия при различных значениях среднего температурного
уровня процесса адиабатического превращения синтез-газа исходного состава в
синтез-газ требуемого состава.
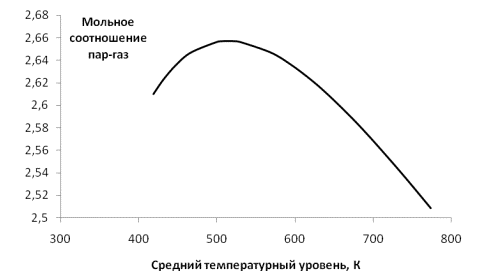
Рис.
2 Оптимальные значения мольного
соотношения пар:газ при различных значениях среднего температурного уровня
(Нижняя граница интервала температур ограничена температурой испарения воды).
Для
выбора окончательного решения представим зависимость критерия ![]() для процессов, представленных на диаграмме рис.2 в зависимости от среднего температурного
уровня процесса (рис.3).
для процессов, представленных на диаграмме рис.2 в зависимости от среднего температурного
уровня процесса (рис.3).
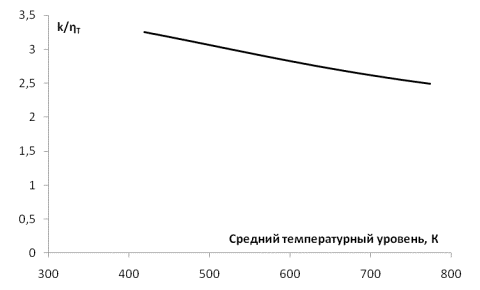
Рис.3 Зависимость критерия второго уровня (![]() ) от среднего температурного уровня процесса
) от среднего температурного уровня процесса
Как следует из
зависимости на рис.3, минимальное
значение критерия оптимальности (минимум) смещается в сторону
высокотемпературной конверсии.
Литература
1. Налетов, В.А. Оптимальная организация химико-технологической системы
на основе декомпозиции задачи по иерархическим уровням. Информационный подход [Текст]/ Налетов В.А., Глебов М.Б., Налетов А.Ю. // Kluczowe Aspekty Naukowej Działalności
– 2014: materiały X międzynarodowej naukowi-praktycznej konferencji. Volume 19. Ekologia. Chemia i chemiczne
technologie. / Przemyśl: Nauka i studia, 2014. – c. 60-64.
2. Налетов, В.А Информационно-термодинамический
принцип организации химико-технологических систем [Текст]/ В. А. Налетов, Л.С.
Гордеев, М.Б. Глебов, А.Ю. Налетов // Теоретические
основы химической технологии ТОХТ. - 2011. - том 45, № 5. - с. 541–549.
3. Справочник азотчика:
Физико-химические свойства газов и жидкостей. Производство технологических
газов. Очистка технологических газов. Синтез аммиака. 2-е изд., перераб. М.: Химия, 1986. – 512 с.