Технические науки/12.Автоматизированные
системы управления на производстве
Ладієва Л. Р., Олійник В. В.
Національний технічний університет України «КПІ»
СИСТЕМА
АВТОМАТИЗОВАНОГО УПРАВЛІННЯ ПРОЦЕСОМ ОТРИМАННЯ ОЦТОВОЇ КИСЛОТИ
Розроблена система
автоматичного управління процесом виробництва оцтової кислоти. Особливістю
цього процесу є те, що кислоту отримують за допомогою процесу окислення
ацетальдегіду.
Однією з важливих причин
розроблення схеми автоматичного регулювання процесу виробництва оцтової кислоти
є досягнення високоякісного кінцевого продукту.
Автоматичне регулювання
дозволяє керувати виробництвом оцтової кислоти за допомогою засобів
автоматизації, забезпечує високу точність керування технологічним процесом та
дає змогу підвищити продуктивність процесу.
Окислення ацетальдегіду проходить в дві
фази. Спочатку утворюється надоцтова кислота (гідро перекис ацетилу) яка,
реагуючи з другою молекулою ацетальдегіду, утворює оцтову кислоту.
Надоцтова кислота є нестійкою сполукою, здатною легко
розпадатися.
Розпад її супроводжується виділенням
великої кількості тепла, а тому нагромадження надоцтової кислоти в продуктах
реакції може спричинити вибух. Крім того, кисень, що виділяється, енергійно
окислює ацетальдегід з утворенням двоокису вуглецю й води.
Щоб запобігти нагромадженню надоцтової
кислоти, підбирають такі каталізатори процесу, в присутності яких обидві фази реакції
окислення проходять з однаковою швидкістю. Деякі каталізатори (наприклад, солі
заліза, міді, кобальту) прискорюють окислення альдегіду в надоцтову кислоту,
але недостатньо підвищують швидкість другої фази – утворення оцтової кислоти.
Застосування як каталізатора ацетату марганцю або комбінованого кобальт
марганцевого каталізатора усуває цей недолік, оскільки солі марганцю сприяють
відновленню надоцтової кислоти в оцтову.
На рисунку показано одну з головних
частин технологічної схеми виробництва оцтової кислоти окисленням
ацетальдегіду.
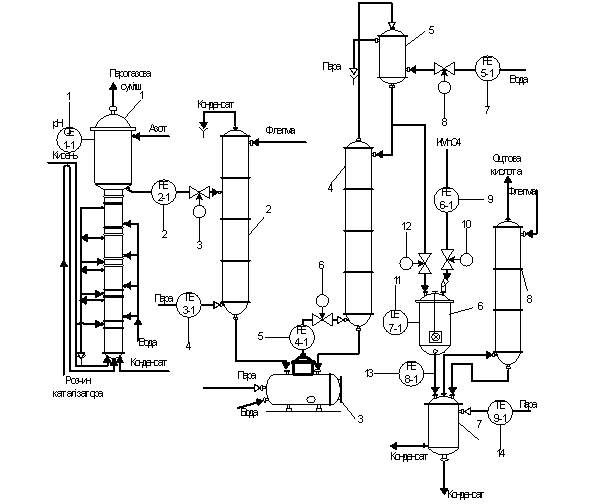
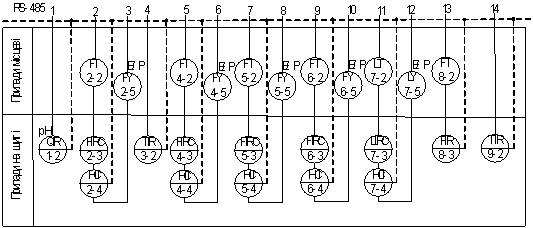
Схема автоматизації процесу виробництва оцтової кислоти
окисленням ацетальдегіду
Оцтова кислота (сирець) безперервно відбирається з
розширеної частини окислювальної колони 1 в якій вимірюється концентрація (поз.
1-1) оцтової кислоти. Її витрата вимірюється первинним перетворювачем –
діафрагмою (поз. 2-1) і регулюється
на вході у ректифікаційну колону 2 за допомогою автоматичного показувального,
реєструвального і керувального вторинного приладу
(поз. 2-3).
Оцтова кислота надходить
у колону 2, де із сирцю, вимірюючи температуру парів (поз. 3-1) з індикацією і реєстрацією цього
значення (поз. 3-2), ці пари надходять з кип’ятильника в нижню частину
ректифікаційної колони і відганяють низькокиплячі сполуки. Звільнена від низькокиплячих сполук кислота безперервно
надходить в кип’ятильник 3 ректифікаційної колони 4, де при 125 °С оцтова
кислота випаровується, відокремлюючись від каталізатора, парів альдегіду,
кротонової кислоти і продуктів осмолення. На виході з кип’ятильника вимірюється
(поз. 4-1) витрата кислоти і
регулюється за допомогою регулятора (поз. 4-4), яка випаровується.
Пари оцтової кислоти
конденсуються у дефлегматорі 5, на вході якого для забезпечення оптимального
температурного режиму регулюється (поз. 5-4) витрата охолоджувальної суміші. З дефлегматора
частина кислоти повертається у вигляді флегми на зрошення колони 4, деяка кількість
спрямовується в апарат для виготовлення каталізаторного розчину, а більша
частина надходить для очищення від домішок в реакторі 6 (в ньому контролюється
рівень суміші контуром 7 на схемі автоматизації, що містить вимірювальний (поз.
7-1) і передавальний (поз. 7-2) пристрої, вторинний показувальний та керувальний
пристрій (поз. 7-3), блок ручного управління (поз. 7-4) та електро-пневматичний
перетворювач сигналу (поз. 7-5), який перетворює електричний сигнал на пневматичний
і передає його на пневматичний виконавчий механізм (поз. 7-6)). Тут оцтову
кислоту обробляють перманганатом калію для окислення домішок, що містяться
в ній. Витрата перманганату калію
контролюється (поз. 6-3) на вході в реактор. Після окислення домішок в реакторі
на виході вимірюється витрата вихідної сировини (поз. 8-1). Для відокремлення
ацетату марганцю, що утворився, кислоту знову випаровують за температури 120 °C…125 °C у випарнику 7, на вході якого вимірюється температура
нагрівної пари (поз. 9-1) з індикацією і реєстрацією цього значення (поз. 9-2).
Звідси її пари надходять в насадочну колону 8.
Література:
1. Юкельсон И. И. Технология
основного органического синтеза [Текст] / И.И. Юкельсон. – М.: «Химия», 1968 –
848 с.: ил. – Библиогр.: с. 401 – 408. – 30000 экз.
2.
Анисимов И. В. Автоматическое регулирование процесса ректификации [Текст]/ И.
В. Анисимов. – М.: «Гостоптехиздат», 1961. – 179 с.: ил. – Библиогр.: с. 6–20.
– 3275 экз.