Садуакасова А.Т., д.т.н. Самойлов В.И., Кожанбердинов
А.Н.
Восточно-Казахстанский государственный технический университет им. Д. Серикбаева,
Казахстан
Извлечение урана из руд и их концентратов гидрометаллургическими способами
В промышленной практике
вскрытие урановых руд осуществляют двумя методами: кислотным и карбонатным
[1-5]. Выбор метода зависит от характера руды. Кислотный метод вскрытия
применяют для урановых руд, в которых уран химически связан с
труднорастворимыми оксидами титана, тория, ниобия, тантала и элементов редких
земель, а также руд с содержанием в них гипса и сульфидов. Для руд, у которых
минералы пустой породы состоят из доломита, кальцита и магнезита,
преимущественно используют карбонатное выщелачивание.
Кислотное
выщелачивание.
Для кислотного выщелачивания урановых руд
в основном пригодны растворы серной кислоты. Применение её основано на том, что
при взаимодействии серной кислоты с шестивалентным ураном образуются
растворимые соединения по реакциям:
UO22+
+ SO42– = UO2SO4,
UO22+
+ 2SO42– = [UO2(SO4)2]2–,
UO22+
+ 3SO42– = [UO2(SO4)3]4–.
Общий
расход кислоты на выщелачивание урана и растворяющихся примесей определяется
как минералогическим составом исходного сырья, так и режимом процесса
выщелачивания. По данным заводской практики расход кислоты обычно составляет
от 30 до 80 кг на 1 т урановой руды. При этом основная доля расхода кислоты
приходится на растворение примесей, хотя для высококремниевых урановых руд
относительный переход примесей в раствор не велик. По данным [1-3], в раствор
переходят 1 % кремния в форме H2SiO3, 1 % кальция в форме CaSO4, 3÷5 % алюминия в форме Al2(SO4)3, 5÷8 %
железа (III) в форме Fe2(SO4)3 и 40÷50 %
железа (II) в форме FeSO4.
Вследствие того, что карбонаты кальция и
магния реагируют с серной кислотой практически полностью, применение кислотного
выщелачивания при содержании их выше 5 % нерентабельно. Рациональнее в таких
случаях либо использовать карбонатное выщелачивание, либо предварительно
удалять из руды карбонаты флотационным или другим методом.
В растворы при
выщелачивании также переходят некоторые количества ванадия, меди, никеля,
хрома и других элементов в виде соответствующих сернокислых солей.
Так как уран в рудах, как правило,
находится не только в хорошо растворимом в растворах серной кислоты
шестивалентном состоянии, но и в труднорастворимом четырёхвалентном, в
производственной практике используют различные окислители: азотную кислоту,
нитрат натрия, пиролюзит и хлорид натрия. В промышленных условиях расход MnO2 или NaClO3 соответственно
составляет 4,5 и 1,25 кг на 1 т руды.
Скорость растворения урановых руд в
значительной мере зависит от температуры. Так выщелачивание урановой смолки при
40 °С в течение 4 ч даёт
такое же извлечение (93 %), как выщелачивание при 25 °С в течение 12 ч. Для руд,
содержащих труднорастворимые урановые минералы, температуру повышают до 50÷60 °С.
При сернокислотном
выщелачивании главное внимание обращается на избирательность растворения
урановых минералов. Это достигается регулированием кислотности на минимально
возможном уровне, регулированием конечного значения рН среды, и выщелачивании
при низких температурах. В ряде случаев использование способов повышения
избирательности приводит к увеличению общего времени выщелачивания. Однако
получение более чистых конечных растворов при более низких расходных
коэффициентах по кислоте делает
использование рассматриваемых способов экономически целесообразным.
Для получения более чистых растворов по
примесям и снижения удельного расхода кислоты в современной урановой
промышленности широко используют принципы стадийного выщелачивания, схемы
выщелачивания оборотными растворами.
В ряде случаев
применяют двойной цикл выщелачивания (рис. 1) при малой кислотности в течение 2÷3 ч в жидкой пульпе, содержащей
20÷25 % твёрдого. Полученная после
выщелачивания пульпа разделяется на твёрдую и жидкую фазы в сгустителях.
Верхний слив сгустителя направляют в цикл ионообменной сорбции, а нижний,
содержащий до 60 % твёрдого выщелачивается в жёстких условиях растворами с
высоким содержанием кислоты (до 60 г/л) и
при повышенных температурах (50 °С). Полученный
кислотный раствор используют для
Урановая Оборотный
![]()
![]()
![]() руда раствор
руда раствор
![]()
Выщелачивание при
малой
конечной
кислотности
![]()
![]()
![]() Сгущение
Осветлённый раствор
Сгущение
Осветлённый раствор
![]() MnO2 на ионообменную
сорбцию
MnO2 на ионообменную
сорбцию
H2SO4 Сгущённая
![]()
![]() пульпа
пульпа
![]() Выщелачивание в жёстких условиях
Выщелачивание в жёстких условиях
![]()
![]() Сгущение
Сгущение
Сгущённая Кислый
![]()
![]() пульпа раствор
пульпа раствор
![]()
![]() Промывка
Промывка
В отвал
Рисунок 1 – Двухстадийная
схема выщелачивания урановых руд растворами серной кислоты
выщелачивания новых порций руды. Осадок,
после тщательной отмывки от растворимого урана, направляется в отвал.
В качестве аппаратов в
цикле выщелачивания применяют пачуки и реакторы с механическим
перемешиванием.
Обычно в результате сернокислотного
выщелачивания получают растворы, содержащие, г/л: 0,6÷1,7 U; 0÷5 V2O5; 2,7÷7 Fобщ; 1÷12 Al; 0,08÷0,4 TiO2; 30÷40 SO42-; 1,2÷1,4 PO43-.
Из таких растворов можно выделить уран в
осадок, в котором будет содержаться до 8 % U. Однако методы сорбционной и
экстракционной очистки растворов от примесей, которые в настоящее время
используют на стадии переработки растворов, позволяют получать более чистые
концентраты урана, в большей степени очищенные от примесей.
В качестве примера технологии с
сернокислотным выщелачиванием и ионитным выделением урана можно привести технологическую
схему канадского завода в Биверлодже, перерабатывающую рядовую смоляную руду
(рис. 2).
Сгущённая пульпа
H2SO4, NaClO3 (после измельчения)
![]()
![]()

Выщелачивание H2SO4
![]()
![]()
Очистка раствора активированным углем 1-я репульпация H2O
![]()
![]()
![]()
![]() HNO3 Ионный обмен 2-я репульпация
HNO3 Ионный обмен 2-я репульпация
![]()
![]()
![]()
![]() Фильтрат на сброс Остаток в отвал
Фильтрат на сброс Остаток в отвал
Элюирование из смолы
![]()
![]() MgO
MgO
![]()
Осаждение урана
![]()
Урановый концентрат
на тонкую химическую очистку
Рисунок 2 – Схема
извлечения урана из руд на канадском заводе Биверлодже
Такая схема принята на всех канадских
заводах, где есть кислотное выщелачивание. Причём на заводах, перерабатывающих
руды с хорошо индивидуализированными урановыми минералами, в состав
технологической схемы обычно включают гравитационное обогащение, а при наличии
более 5 % сульфидных минералов предусмотрено их отделение флотацией. На заводах
в Биверлодже (Канада) и Блайд Риве (США) гидрометаллургической обработке
предшествует операция измельчения руды до крупности класса -0,074 мм
(55÷65 %), в то время как для банкрофских руд (США) оказывается
достаточным измельчение до крупности класса -0,074 мм (40 %). Если измельчённая
руда плохо сгущается, и продукт, выдаваемый сгустителями, содержит меньше
55÷60 % твёрдого, пульпу уплотняют на вакуум-фильтрах. В Канаде
выщелачивание ведут серной кислотой с добавкой в качестве окислителя хлората
натрия, а на заводах США окисление
проводят преимущественно пиролюзитом. Расход кислоты в зависимости от состава
руд и, в частности, от количества карбонатных минералов колеблется от 30 до 80
кг/т. Обычно температура выщелачивания составляет 40÷45 °С, а объём маточного
раствора, поступающего в ионообменные колонки, 1,5÷1,75 м3
на 1 т перерабатываемого материала.
Для получения более чистых урановых
концентратов кислые маточные растворы осветляют с помощью активированного
угля, поглощающего из раствора лишь примеси. Извлечение урана с применением
анионообменных смол обычно ведут при рН = 1,5÷1,8. Десорбцию урана со
смолы выполняют растворами серной или
азотной кислот в смеси с поваренной солью. На десорбцию 1 кг U3O8 расходуют 1÷2 кг кислоты. На осаждение
уранового концентрата затрачивают примерно столько же оксида магния. Извлечение
урана по этой схеме на различных зарубежных заводах колеблется в интервале
84÷94 %.
Карбонатное
(содовое) выщелачивание.
Данный способ
выщелачивания является вторым по значению и распространению методом вскрытия
урановых руд [1-5]. При растворении урановой руды в карбонатных растворах
образуются хорошо растворимые в растворах соды ионы уранилтрикарбоната.
Образование этих ионов, например, при растворении карнотита, в котором уран
находится в шестивалентном состоянии, или уранита, в котором уран находится в
четырёхвалентном состоянии, происходит по следующим реакциям:
![]() K2(UO2)2(VO4)2∙3H2O
+ 6CO22– 2K+ + 2[UO2(CO3)3]4–+
2VO3– + 4OH–
+ H2O;
K2(UO2)2(VO4)2∙3H2O
+ 6CO22– 2K+ + 2[UO2(CO3)3]4–+
2VO3– + 4OH–
+ H2O;
![]() 2UO2 + 6CO32– + O2 2[UO2(CO3)3]4– + 4OH–.
2UO2 + 6CO32– + O2 2[UO2(CO3)3]4– + 4OH–.
Из указанных реакций видно, что в процессе карбонатного выщелачивания в
растворе накапливаются ионы гидроксила, что может привести к осаждению
диураната натрия:
![]() 2[UO2(CO3)3]4– + 6OH– + 2Na+
Na2U2O7 + 6CO32– + 3H2O.
2[UO2(CO3)3]4– + 6OH– + 2Na+
Na2U2O7 + 6CO32– + 3H2O.
Поэтому для
нейтрализации выделяющейся щёлочи растворение ведут в присутствии бикарбоната
натрия:
![]() HCO3–
+ OH– CO32– + H2O.
HCO3–
+ OH– CO32– + H2O.
В горячих растворах карбонатов устойчивым
является комплекс, в котором уран находится в шестивалентном состоянии.
Поэтому если в минералах уран находится в четырёхвалентном состоянии,
растворение необходимо проводить в присутствии окислителя. В производственных
условиях в качестве окислителя используют кислород. Окислителями также могут
служить перманганат калия или гипохлорит натрия.
При карбонатном
выщелачивании уран отделяется от большей части нежелательных примесей. В
определённых условиях катионы редкоземельных элементов, меди, никеля,
кобальта, кадмия и др., а также анионы, образованные фосфором, бором,
мышьяком и др., не осаждаются при выделении урана из растворов.
При организации
карбонатного выщелачивания следует учитывать, что, если в исходной руде
содержится более 4 % сульфидов, то применение этого способа нерентабельно из-за
больших безвозвратных потерь соды. Поэтому для таких руд, если нельзя из них
предварительно удалить сульфиды, например, флотацией, следует использовать
кислотное выщелачивание.
В производственных
условиях уран извлекают из карбонатных растворов осаждением гидроксидом натрия
в виде диураната натрия. В ряде случаев уран из содовых растворов осаждают в
виде диураната аммония. Наиболее полно диуранаты аммония и натрия осаждаются
при рН = 5÷6. Практика аммиачного осаждения сводится к прогреванию
раствора для удаления СО2 для последующей лучшей коагуляции осадка.
При 60÷80 °С в течение 1,5÷2,0 ч при интенсивном перемешивании
в исходный раствор постепенно добавляют водный раствор аммиака, содержащего до
25 % масс. NH3. Процесс осаждения может быть осуществлён как в периодическом, так и в
непрерывном вариантах. Аналогичен процесс осаждения урана из растворов с
применением натриевой щёлочи.
Маточные растворы
после регенерации снова используют для выщелачивания новых порций руды.
Регенерация происходит в результате пропускания через маточные растворы
углекислого газа и образования в них карбоната и бикарбоната:
2NaOH +
CO2 = Na2CO3 + H2O;
Na2CO3
+ CO2 + H2O = 2NaHCO3.
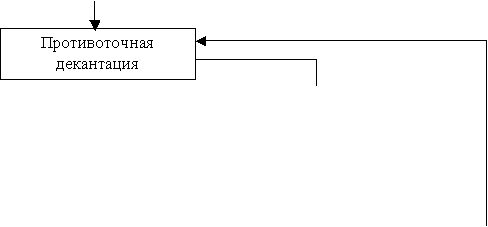
На рис. 3 приведена
типичная схема карбонатного выщелачивания урана из руд Биверлоджа (Канада).
Условия осуществления данного процесса следующие.
Необходимо более
тонко, чем по кислотной схеме, измельчить материал (примерно до крупности 80
% класс -0,074 мм), т. к. активность растворителя в данном случае ниже. Само измельчение
проводят обычно не в воде, а в 5 %-ном растворе соды. Содовые пульпы, как
правило, сгущаются хуже кислых, поэтому на стадии разделения твёрдой и
жидкой фаз желательно использовать флокулянты – вещества, ускоряющие осветление.
Концентрацию соды в
выщелачивающих растворах поддерживают обычно на уровне 50 г/л при содержании 20
г/л бикарбоната, если выщелачивание ведут в пачуках, и 10 г/л при работе в
автоклавах.
Выщелачивание урана из
руд в пачуках при 75 °С требует до 4 сут. При
Дроблёная руда
![]() Раствор
Раствор
Мокрое измельчение
Na2CO3 и NaHCO3

![]() Сгущённая Слив
Сгущённая Слив
![]() пульпа
пульпа

![]() Воздух
Воздух
![]()
![]()
Шламы
Фильтрация и промывка![]()
Осветлённый
раствор
Н2О
![]() Na4[UO2(CO3)3]
Na4[UO2(CO3)3]
NaOH![]()
![]()
Осаждение![]()
Шлам Раствор
![]()
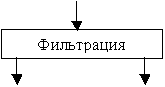
Осадок Раствор
Na2U2O7 Na2CO3,
![]() (урановый NaОН
(урановый NaОН
концентрат)
Регенерация карбонатного раствора
![]() СО2
СО2
![]()
Рисунок 3 – Схема карбонатного
выщелачивания урановых руд
Работе с такими же рудами в автоклавах при
100 °С и подаче воздуха под давлением до 9,8 МПа необходимая
продолжительность сокращается до 16 ч. Обычно извлечение урана по такой схеме
составляет 89÷94 %.
Наряду
с осаждением урана из растворов со стадии карбонатного выщелачивания рудного
сырья, известно об использовании в США
технологии сорбции урана из
указанных растворов с применением сильноосновного анионита IRA-400
(аналогом данной смолы является выпускаемая в России смола AM) [2].
Литература
1. Матвеев Ю.Н., Стрижко В.С. Технология
металлургического производства цветных металлов (теория и практика): Учебник
для вузов. – М.: Металлургия, 1986. – 368 с.
2. Тураев Н.С., Жерин И.И.
Химия и технология урана: Учебное пособие для вузов – М.:ЦНИИАТОМИНФОРМ, 2005.
– 407 с.
3. Смирнов А.Л., Волкович В.А. Переработка облучённого ядерного топлива. Конспект лекций. – Екатеринбург: ГОУ ВПО УГТУ-УПИ, 2008. –
317 с.
4. Маслов А.А. Технология урана и плутония: учебное пособие / А.А. Маслов, Г.В. Каляцкая, Г.Н.
Амелина, А.Ю. Водянкин, Н.Б. Егоров – Томск: Издательство Томского
политехнического университета, 2007. – 97 с.
5.
Вдовенко В.М. Современная радиохимия. – М.: Атомиздат, 1969. – 544 с.