Д.ф.н.
Безуглий П.О., д.х.н. Болотов В.В., к.х.н. Маміна О.О.,
к.ф.н.
Леонова С.Г., Колісник О.В.
Національний
фармацевтичний університет, м. Харків
ВИБІР ОПТИМАЛЬНИХ УМОВ
ХРОМАТОГРАФІЧНОГО АНАЛІЗУ АЛКАЛОЇДІВ
ПРИ ЇХ СУМІСНІЙ ПРИСУТНОСТІ У БІОЛОГІЧНИХ ОБ´ЄКТАХ
Органічні лікарські речовини загального дослідження
при проведенні судово-медичних експертиз (алкалоїди - похідні хіноліну,
піридину та піперидину, ізохінолину та ациклічні алкалоїди) широко застосовуються
у медичній практиці [1].
В літературі
описані чисельні випадки важких та летальних
отруєнь алкалоїдами в
результаті перевищення доз при самолікуванні,
сумісному застосуванні з іншими препаратами та алкоголем, при наркотичній
залежності, а також у випадках суїциду [2,3].
Метою даної роботи є вибір
оптимальних умов аналізу алкалоїдів при їх сумісній присутності у біологічних
об´єктах методом високоефективної рідинної хроматографії на прикладі суміші
алкалоїдів, які відрізнялись за будовою - хінін, анабазин, папаверин та
ефедрин.
Недоліками наведених в літературних
джерелах ВЕРХ-методик аналізу
лікарських речовин є застосування різноманітних умов дослідження (склад рухомої
фази, ізократичне або градієнтне елюювання, детектування при одній або
декількох довжинах хвиль, вибір чутливого та селективного детектору), які базуються
на властивостях обмеженої групи отрут[4-6].
Попередні дослідження нами виконані у напрямках вибору органічної
фази елюенту (метанол, ацетонітрил), складу та рН буферного розчину (6,0-7,0;
2,0-3,0), застосування іон-парного агента (літію перхлорат), режиму надання
елюенту у колонку (ізократичний або градієнтний) при температурі колонки –35 - 37°С; тисненню
насосу – 2,6 – 2,8 МПа; об´єму проби для
введення– 1-5 мкл
(концентрація розчинів речовин -
10-100 мкг/мл) (схема).
Схема
Вибір умов аналізу речовин ВЕРХ-методом
Мікроколоночний рідинний хроматограф “Міліхром А-02”, металева колонка 2х75мм з сорбентом Nucleosil – 100 – 5, C18
Склад
рухомої фази та режим надання елюенту у колонку
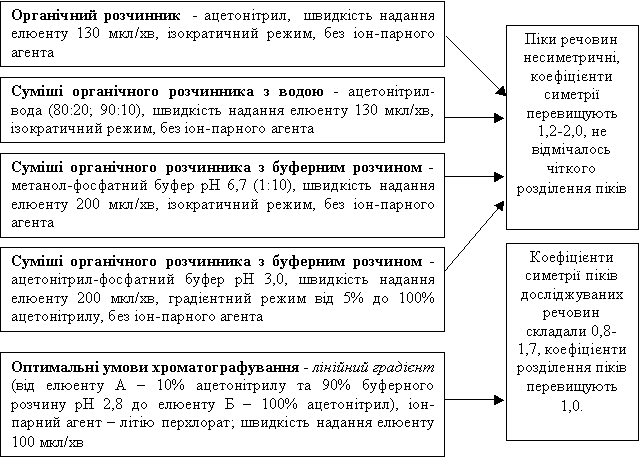
В результаті досліджень була розроблена
ВЕРХ-методика, придатна для ідентифікації, кількісного визначення та скринінгу
індивідуальних отрут та їх сумішей у біологічних об´єктах.
При аналізі застосовували багатоканальне
детектування речовин за 7 довжинами хвиль – 210, 230, 240, 260, 280, 300 та 330
нм, при цьому кожній речовині на хроматограмі відповідали 7 піків з однаковим часом утримування, але з різними
амплитудами, прямо пропорційними екстинкції речовини.
В результаті
ВЕРХ-досліджень нами отримані симетричні піки, гострі за формою, що
обумовлювало можливість проводити надійну обробку хроматограм (рис.).
![]()
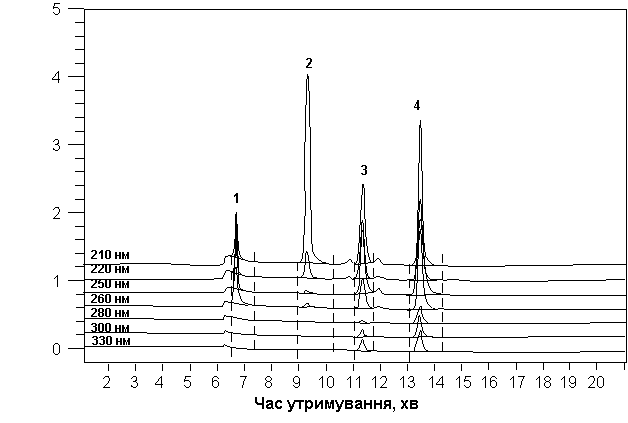
Рис. Хроматографічне розділення суміші
алкалоїдів, похідних різних
гетероциклів: 1 – анабазину (10,0 мкг/мл); 2 – ефедрину
(50,0
мкг/мл); 3 – хініну (25,0
мкг/мл); 4 - папаверину (50,0 мкг/мл).
Ідентифікацію алкалоїдів проводили за
параметрами утримування та спектральними
відношеннями, які були визначені як відношення значень оптичної густини при 6 довжинах хвиль – від 230 до 330 нм – до
значень оптичної густини при 210 нм (табл. 1)[4].
Встановлено, що спектральні відношення при 300 та 330 нм характеризуються
низькими значеннями у порівнянні зі спектральними відношеннями при інших
довжинах хвиль, що надавало можливості ці дані не враховувати.
Коефіцієнти симетрії піків досліджуваних
речовин складали 0,8-1,7, що відповідало оптимальним значенням коефіціентів
симетрії піків - менше 2,0 –2,5. Розраховані значення коефіціентів ємності були
у межах від 3,33 до 10,55 при оптимальному інтервалі значень коефіціентів
ємності – від 2 до 10, що свідчило про придатність хроматографічної системи.
Таблиця 1.
Параметри
утримування та спектральні відношення алкалоїдів (n = 5)
|
Речовини |
Параметри утримування речовин |
Границя
визначення - Gmin, мкг/мл |
Коефіцієнт
ємності, k´ |
|||
|
tабс, хв |
Vабс, мкл (tабс·w) |
|
||||
|
Анабазин |
6,50+0,03 |
650 |
1,0 |
3,33 |
|
|
|
Ефедрин |
9,14 + 0,02 |
914 |
2,2 |
5,09 |
|
|
|
Папаверин |
13,07 + 0,02 |
1307 |
1,7 |
7,71 |
|
|
|
Хінін |
11,36 +0,03 |
1136 |
1,6 |
6,57 |
|
|
|
Спектральні відношення |
|
|||||
|
|
А 210 нм |
А 210 нм |
А 210 нм |
А 210 нм |
|
|
|
Анабазин |
0,114 |
1,230 |
1,815 |
-0,011 |
|
|
|
Ефедрин |
0,002 |
0,008 |
0,020 |
-0,001 |
|
|
|
Папаверин |
0,961 |
2,802 |
1,245 |
0,292 |
|
|
|
Хінін |
0,621 |
0,936 |
0,356 |
0,038 |
|
|
|
||||||
Для оцінки хроматографічного розділення
сумішей розраховували: коефіцієнт симетрії піку, селективність, коефіцієнт розділення піків (табл.2).
Встановлено,
що практично для досліджуваних
речовин селективність складає 1,07-2,35; коефіцієнти розділення піків
перевищують 1,0; коефіцієнти симетрії піків не перевищують 2,0.
Таблиця 2
Основні хроматографічні параметри розділення піків алкалоїдів
|
Речовини |
Селективність,
α |
Коефіцієнт
розділення піків, Rs |
Число теоретич-них тарілок, n |
Коефіцієнт
симетрії |
||
|
Анабазин |
- |
- |
- |
- |
995 |
1,07 |
|
Ефедрин |
1,50-a 3,1 |
- |
- |
3,09 - Rs 2,1 |
1925 |
1,75 |
|
Хінін |
1,89-a 3,1 |
1,26-a 3,2 |
- |
2,40 - Rs 3,2 |
2855 |
1,47 |
|
Папаверин |
2,29-a 4,1 |
1,53-a 4,2 |
1,16-a 4,3 |
2,44 - Rs 4,3 |
3991 |
1,50 |
Таким чином, одержані результати свідчать про придатність вибраних оптимальних умов хроматографування для розділення та аналізу багатокомпонентних сумішей нативних речовин у біологічних об´єктах.
Література
1. Машковский М.Д. Лекарственные средства: в 2-х т., Т.1.– М.: ООО «Изд-во
«Новая волна», 2000.– 540с.
2. Randall C. Disposition of Toxic Drugs and
Chemicals in Man / Chemical Toxicology Institute.– Foster City, 2000.– 918 p.
3. Fatal
blood and tissue concentrations of more than 200 drugs / F. Musshoff, S.
Padosch, S. Steinborn et al. // Forensic.
Sci. Internation. – 2004.– Vol.142, № 2-3. – P. 161-210.
4. Baram
G.I. Portable liguid chromatograph for mobile laboratories // J. Chromatogr. А.
– 1996.– Vol.728, № 3. – P.387-399.
5. High
perfomance liquid chromatography in pharmaceutical analyses / B. Nicolin, B.
Imamovic, S. Medanhodzic-Vuk, M. Sober // Bosn J. Basic Med. Sci. – 2004. -
Vol. 4, № 2. – P. 5-9.
6. Herzler M.
Selectivity of substance identification by HPLC-DAD in toxicological analysis
using a UV spectra library of 2682 compounds // J. Anal. Toxicol. – 2003.-
Vol.27, № 4. – P. 233-242.