Химия и химические технологии/
6.Органическая химия.
К.х.н. 1 Валюк В.Ф., к.х.н. 2 Шилін С.В.
1Уманський
державний педагогічний університет
ім. Павла Тичини, природничо-географічний факультет, кафедра хімії та екології, 02003,
Україна, Умань, вул. Садова 2, e-mail: Vvalyuk@mail.ru
2 Київський
національний університет імені Тараса Шевченка, хімічний факультет, кафедра
органічної хімії. 01033 Україна, Київ, вул. Володимирська, 64.
Основні методи одержання кумаринів
Існує ціла низка різноманітних методів синтезу кумаринової системи,
включаючи реакцію Перкіна [1-2], Пехмана [3], конденсацію Кневенагеля [4], а
також реакцію Реформатского [5] або Віттіга [6] та ряд інших підходів, що
дозволяє отримувати різноманітні похідні кумарину.
Вперше кумарин 1.1 було синтезовано конденсацією за Перкіним при взаємодії саліцилового
альдегіда 1.2 (схема 1.1) з оцтовим ангідридом в
присутності ацетата натрія.
Схема
1.1
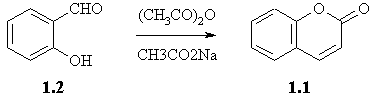
Крім лужних ацетатів в реакції Перкіна можуть бути застосовані й інші каталізатори основного характера, наприклад, триетиламін. Перетворення заміщених саліцилових альдегідів на кумарини часто супроводжується
осмоленням, що зумовлює невисокий вихід відповідних похідних [7].
Якщо замість оцтового ангідриду використовувати ангідриди та солі інших аліфатичних кислот
– фенілоцтової, метоксиоцтової, феноксиоцтової тощо – то утворюються 3-заміщені похідні
кумарину 1.3 (схема 1.2).
Схема 1.2
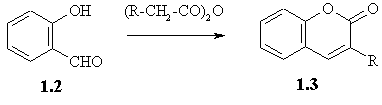
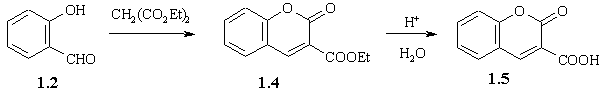
Однак більш високий вихід 3-заміщених похідних
кумарину спостерігається внаслідок реакції Кневенагеля [4] тобто конденсації альдегідів або кетонів із сполуками, що мають
активовану метиленовцу групу (схема
1.3). Реакція відбувається з похідними малонової кислоти, а також з менш реакційноздатними сполуками, наприклад, з гліцином або гіпуровою кислотою, що дозволяє синтезувати 3-амінокумарини [7].
Схема 1.3
Похідні
малонової кислоти можна використовувати і у випадках,
коли реакція Перкіна не йде. Цей метод застосовують, наприклад, для одержання 5-гідроксикумаринів [7].
Однак найбільш розповсюдженим методом синтезу кумаринів є реакція Пехмана [3], для якої характерні високі виходи різноманітних заміщених похідних
кумарину з порівняно простих вихідних речовин. Реакція Пехмана полягає у взаємодії
фенолів 1.6 з β-кетоестерами 1.7 в присутності сильних кислот Бренстеда (наприклад,
метансульфокислоти) або кислот Льюіса (AlCl3, ZnCl2) (схема
1.4). Спочатку для цієї конденсації використовували сірчану кислоту, а потім і інші
конденсуючі агенти: фосфорну кислоту, розчин хлористого водню в оцтовій кислоті або спирті, трифтороцтову
кислоту, Р2О5, тіоніл хлористий, борний ангідрид, хлорокис фосфора чи титана,
ацетат міді, етилат натрію. В якості каталізаторів застосовувались також цеоліти [8], глини та катіонообмінні смоли (Dowex 50х2, Amberlyst, Zeocarb 225 та
інші) [7, 8].
Схема 1.4
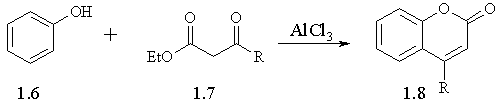
При конденсації фенолів та β-кетоестерів різної будови можна одержати
кумарини, що містять різноманітні радикали у бензольному кільці,
гетероциклічному ядрі, або одночасно в обох кільцях [3].
Механізм реакції Пехмана (схема 1.5) полягає в тому, що кислота каталізує
процеси транс-естерифікації (що дає сполуку 1.9) і кето-єнольної
таутомерії (яка веде до продукту 1.10). Подальше приєднання за Міхаелем
обумовлює утворення скелету кумарину. Каталізовані кислотою процеси наступної
ароматизації та відщеплення води приводять до утворення кінцевого продукту 1.8 [3].
Схема 1.5
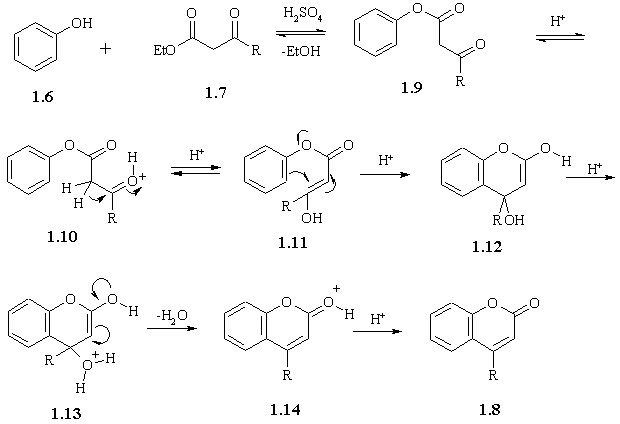
Напрямок реакції визначається наявністю замісників у
молекулі фенолу, структурою β-кетоестеру й природою конденсуючого агенту [3, 7].
Із моно- ди- та триатомних фенолів найбільшу реакційну
здатність виявляє резорцин, який здатен вступати в реакцію з багатьма естерами
заміщених β-кетокислот. Ефективність утворення кумаринів залежить також
від положення замісників у фенолів [3]. Так, феноли, що мають у мета-положенні
гідрокси-, метокси-, аміно-, діалкіламіно-, або алкільну групу вступають у
реакцію Пехмана значно легше самого фенолу [3, 7]. Що стосується замісників
β-кетоестерів, то угруповання, які сприяють енолізації або стабілізують
енольну форму дикетонів обумовлюють більш ефективне протікання реакції [3, 7]. Для синтезу кумаринів з високими
виходами використовувались також полімерні естери ацетооцтової кислоти.
Конденсуючі реагенти також сильно впливають на ефективність та напрямок
протікання реакції Пехмана. Наприклад, феноли, які не дають кумарини в
присутності концентрованої сірчаної кислоти, можуть утворювати хромони під впливом Р2О5. Було
також знайдено, що з POCl3 іноді спостерігаються кращі результати, ніж з
концентрованою сірчаною кислотою [3, 7]. Нещодавно було показано, що час
реакції різко зменшується, якщо процес вести у середовищі іонної рідини:
1-бутил-3-метилімідазолій хлоралюміната. Ця сполука грає подвійну роль,
виступаючи як в якості розчинника, так і каталізатора Льюіса
[6]. Запропоновано ефективний метод синтезу 4-заміщених похідних 1.8 з
використанням BiCl3 без розчинників, що дає відповідні гетероцикли с високими виходами [7].
За останні роки для прискорення реакції та підвищення
виходу кумаринів широке застосування знайшла методика, за якою використовують
мікрохвильове опромінення вихідних реагентів. Цей прийом значно скорочує час
реакції від декількох годин до декількох хвилин та підвищує, як правило, вихід
продуктів реакції.
Література:
1.
Кузнецова Г.А. Природные кумарины и фурокумарины.-
Ленинград: «Наука», 1967 – 248с.
2.
Johnson J.R. The
Perkin reaction and related reactions. // Organic reactions.- NY.: John Willey
& Sons, 1942, vol. 1.- P. 210-265.
3.
Sethna S., Phadke R. The Pechmann reaction. // Organic reactions.- NY.: John Willey &
Sons, 1953.- vol. 7.- P. 1-58.
4.
Jones G. The
Knoevenagel condensation. // Organic reactions.- NY.- London – Sydney: John
Willey & Sons, 1967.- vol. 15.- P. 204-599.
5.
Shrimer R. The
Reformatsky reaction. // Organic reactions.- NY.: John Willey & Sons,
1942.- Vol. I.- P. 1-37.
6.
Narasimhan N.S., Mali E.S., Barve M.V. Synthetic application of lithiation reaction: Part XIII. Synthesis of
3-phenylcoumarins and their benzo derivatives. // Synthesis.- 1979. - № 11. - P.
906-908.
7.
Вавзонек С. Кумарины. // Гетероциклические соединения. М.: Изд-во иностранной литературы, 1954.- Т.2.-
С. 134-168.