ПОРАЖЕНИЕ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ У ДЕТЕЙ С
МУКОВИСЦИДОЗОМ
Булатов В.П., Рылова Н.В.
Казанский государственный медицинский университет
Муковисцидоз (МВ) – наследственное заболевание,
вызывающее поражение преимущественно дыхательной и пищеварительной систем,
которое приводит к развитию экзокринной недостаточности поджелудочной железы.
Синдром мальабсорбции обнаруживается
практически у всех больных МВ и проявляется уже в период
новорожденности, но остается на заднем плане, так как большее внимание
уделяется коррекции бронхолегочных процессов.
В клинической картине муковисцидоза (МВ) доминируют
бронхолегочные изменения, определяя течение и прогноз заболевания. Однако
поражение системы пищеварения, прежде всего поджелудочной железы, существенно
влияет как на состояние больных, так и на качество их жизни. Нарушается
нормальное всасывание нутриентов,ч что приводит к нарушению метаболизма
незаменимых жирных кислот класса омега-3 и омега-6 (линолевой,
альфа-линоленовой, декозогексаеновой, эйкозопентаеновой, арахидоновой кислот),
дефициту многих жирорастворимых витаминов и других нутриентов. Панкреатическая
недостаточность, даже при существенном снижении экзокринной функции,
клинически не проявляется, поскольку резервный потенциал поджелудочной железы
чрезвычайно велик и позволяет компенсировать недостаток ферментов вплоть до 90%
утраты функциональных
возможностей [1]. Следовательно, только лишь на основании клинических симптомов
нельзя делать вывод о наличии или отсутствии внешнесекреторной недостаточности поджелудочной железы –
для этого должны быть использованы более надежные инструментальные и
лабораторные методы. Необходима ранняя диагностика изменений поджелудочной
железы при муковисцидозе для начала своевременного лечения, повышения
терапевтического эффекта и улучшения прогноза заболевания.
Структурные изменения поджелудочной железы можно
диагностировать с помощью ультразвукового исследования, компьютерной томографии
и магнитно-резонансной томографии. Множественные микроскопические или небольшие
макроскопические ретенционные кисты являются типичным патоморфологическим
проявлением муковисцидоза. Эти кисты развиваются в результате обструкции
протоков поджелудочной железы вязким секретом. Обычно их размер не превышает 1
– 3 мм в диаметре, в редких случаях встречаются кисты больше 10 мм. В
большинстве случаев кистоз поджелудочной железы при муковисцидозе асимптомен,
однако некоторые авторы описывают его воспалительный компонент [2]. М.И. Пыков
с соавт. (2001) считают, что в детском возрасте характерные для этого
заболевания кисты не видны. При первом ультразвуковом исследовании заключение о
хроническом панкреатите не выносится. Только при повторной эхографии спустя 6-12
месяцев на фоне целенаправленной терапии при сохранении всех изменений
паренхимы можно выносить заключение о хроническом процессе [3]. По мнению И.В.
Дворяковского и соавт. (2008), оценка состояния поджелудочной железы обычно
ограничивается описанием ее размеров, контуров и неоднородностью паренхимы без
уточнения характера этих изменений. Выявление кист диаметром менее 1 мм в
поджелудочной железе должно давать врачу основание заподозрить муковисцидоз и
провести дополнительное обследование для его исключения или подтверждения [4].
По данным Г.В Римарчук и соавт. (1999), при
ультразвуковом исследовании поперечных размеров головки, тела и хвоста
поджелудочной железы натощак и через 1,5 – 3 часа после физиологического
завтрака по приросту суммы линейных размеров до и после еды можно
диагностировать хронический панкреатит, если размеры ПЖ уменьшились или
увеличились не более чем на 5%, реактивный панкреатит – при увеличении размеров
на 6-15%, а при увеличении более чем на 16% диагностируют реакцию ПЖ как соответствующую
норме [12].
При проведении компьютерной томографии возможно
выявить целый спектр изменений, который также зависит от давности заболевания.
У пациентов с минимальными нарушениями экзокринной функции органа могут быть
менее выраженные изменения, такие как липоматозная инволюция, в то время как у
пациентов с ярко выраженной экзокринной недостаточностью и длительной давностью
заболевания отмечается значительное уменьшение размеров и фиброзные изменения
поджелудочной железы. Плотность поджелудочной железы может быть столь высокой,
что возникают большие сложности в дифференцировке органа от окружающей ткани.
Размеры поджелудочной железы уменьшаются вследствие прогрессирующего фиброза.
Наиболее выраженные изменения поджелудочной железы свойственны детям с
умеренной легочной симптоматикой и преимущественно кишечной формой заболевания
[5].
«Золотым стандартом» для
диагностики заболеваний поджелудочной железы считается эндоскопическая
ретроградная панкреатохолангиография. Однако эта методика имеет ряд противопоказаний,
нередко провоцирует обострение панкреатита и проводится только в условиях
специализированных клиник.
Дополнительно
к инструментальному исследованию поджелудочной железы необходимо проводить и
лабораторные исследования, такие как копрологическое исследование,
количественное определение жира в кале, определение ферментов поджелудочной
железы: амилазы, липазы, диастазы, эластазы-1. Многие из
предлагаемых ранее методов (секретин-панкреозиминовый тест, тест Лунда,
ПАБА-тест) не используются у детей в связи с длительностью, инвазивностью и
ограниченной информативностью или неоднозначностью интерпретации результатов.
Определяется активность ферментов, вырабатываемых
поджелудочной железой: амилазы, липазы, фосфолипазы А2, трипсина. Обычно
определяется активность амилазы, которая при обострении хронического
панкреатита увеличивается в 1,5–3 раза. Однако у части больных это увеличение
бывает кратковременным и поэтому не всегда определяется в момент исследования.
Подчеркнем, что амилаза не может рассматриваться, как специфичный маркер
поражения поджелудочной железы, так как может повышаться при заболеваниях
слюнных желез, лёгких, печени, гениталий, почек. Гиперамилаземия встречается
при хронической почечной недостаточности, вирусном гепатите, язвенной болезни
двенадцатиперстной кишки, мезентериальном тромбозе и других заболеваниях. В
силу этого определение общей активности амилазы в сыворотке крови имеет
небольшую диагностическую ценность, особенно в случаях, когда ее уровень бывает
нормальным. При остром поражении поджелудочной железы уровень амилазы в
сыворотке крови достигает максимума ориентировочно через 12 ч, а в моче через
сутки после начала заболевания. Повышение
уровня липазы в биохимии крови имеет большее диагностическое значение, чем
амилазы. Недостатком данного способа является изменение показателей в ответ на
применение заместительной терапии ферментативными препаратами.
Следует также
признать, что копрологическое исследование кала до настоящего времени не
потеряло своей актуальности и является самым доступным методом, способным
подтвердить наличие внешнесекреторной недостаточности поджелудочной железы. При
функциональной недостаточности поджелудочной железы, сопровождающейся дефицитом
или снижением активности панкреатических ферментов, нарушается процесс
расщепления и всасывания пищевых веществ в кишечнике. Это тотчас отражается на
внешнем виде каловых масс:
– стул становится объемным, появляется «полифекалия»;
– каловые массы сероватого цвета, имеют «сальный» вид;
– появляется зловонный, гнилостный запах
[6].
Недостатком
данного метода является то, что исследование кала на копрологию следует
проводить до назначения панкреатических ферментов, что практически невозможно,
так как больные муковисцидозом получают постоянную пожизненную заместительную
терапию ферментативными препаратами. На точность данного метода также влияют:
состояние моторики кишечника, объем выделяемой в просвет кишечника желчи, ее
качественный состав, наличие воспалительных процессов в кишечнике и др.
Содержание
жиров в стуле также оценивается количественным методом. Количественный метод
является наиболее информативным [7]. Этот метод позволяет суммарно определить
общее количество жира в фекалиях с учетом жира экзогенного (пищевого)
происхождения. В норме количество жира, выделяющегося с калом, не должно
превышать 10% введенного с пищей. При заболеваниях поджелудочной железы
количество выделенного с калом жира иногда увеличивается до 60% [8]. Метод
может быть использован для уточнения характера стеатореи, оценки эффективности
ферментотерапии [9].
В настоящее время все более популярным является
проведение ИФА диагностики на определение фермента поджелудочной железы
эластазы 1. Данный фермент определяется как в сыворотке крови, так и в
фекалиях. На сегодняшний день все большую популярность приобретает фекальный
эластазный тест, так как он обладает более высокой специфичностью,
чувствительностью по сравнению с рутинными способами определения экзокринной
недостаточности поджелудочной железы и является неинвазивным способом
диагностики. По данным
Н.И. Капранова с соавт. (2001), чувствительность метода для постановки диагноза
муковисцидоза составила 86,6%, а при выявлении панкреатической недостаточности
у больных с муковисцидозом – 93% [10].
Легкость выполнения, сохранение активности эластазы
при пассаже по кишечнику, отсутствие перекрестных реакций с ферментными
препаратами, возможность использования у детей любого возраста выводят этот
тест на ведущее место среди всех диагностикумов по определению состояния
поджелудочной железы. Кроме того, образцы кала сохраняют стабильность при
температуре 20 C в течение 7 дней, а при температуре 40 С – до 30 дней.
Нормальный уровень эластазы в кале не должен снижаться менее 200 мкг/г. Уровень
эластазы от 200 до 100 мгк/г оценивается как умеренная недостаточность
поджелудочной железы. Если уровень эластазы 1 в кале опускается ниже 100 мкг/г,
значит, у больного выраженная панкреатическая недостаточность. Этот тест может
использоваться для скрининга и мониторинга недостаточности поджелудочной железы
у детей. Однако имеющиеся литературные данные по применению этой методики
противоречивы. Ряд авторов утверждает, что определение фекальной эластазы 1
превосходит по чувствительности другие методы диагностики хронического
панкреатита [11]. Однако полученные при эластазном тесте данные недостоверны в
случае легкого течения заболевания.
Эластаза 1 — протеолитический фермент
поджелудочной железы с молекулярным весом около 28 мДа. Панкреатическая
эластаза 1, благодаря своей высокой биологической стабильности, не изменяет
своей структуры при пассаже через желудочно-кишечный тракт. Поэтому её
концентрация в каловых массах достоверно отражает состояние экзокринной функции
поджелудочной железы. В противоположность общепринятым сегодня лабораторным
параметрам, применяемым для диагностики панкреатита, таких как рутинный
копрологический тест, тест на активность фекального химотрипсина, определение
панкреатической эластазы 1 имеет ряд преимуществ:
– количественное измерение степени
поражения экзокринной функции поджелудочной железы;
– процедура теста позволяет не отменять
ферментативную терапию;
– одного образца кала достаточно для
постановки диагноза (нет необходимости собирать суточный кал);
– высокая стабильность позволяет не
ограничивать время хранения образцов;
В начале 90-х годов немецкой фирмой ScheBo
BioTech был разработан иммуноферментный метод определения панкреатической
эластазы 1 в стуле и в сыворотке крови для выявления хронического и острого
панкреатита (эластаза 1 копрологический тест, кат. №:07 и Эластаза 1
сывороточный тест, кат. №:06) . В последние 10 лет метод определения
панкреатической Эластазы 1 широко применяется во многих клиниках Европы и
Северной Америки у больных с различной патологией желудочно-кишечного тракта.
Тест доказал свою высокую специфичность (95%) и чувствительность (94%). Более
того, результаты данного теста позволяют не только подтвердить или исключить
экзокринную недостаточность поджелудочной железы, но и установить степень ее
поражения.
В основе принципа иммуноферментного
анализа панкреатической эластазы 1 лежит определение специфической эластазы,
характерной только для человека. На дно пластиковых планшет для
иммуноферментного анализа нанесен слой моноклональных антител, которые распознают
исключительно человеческую панкреатическую эластазу 1. Эластаза 1 из
исследуемых образцов присоединяется к антителам и оказывается иммобилизованной
на планшете. Вторые, биотинилированные моноклональные антитела, присоединяются
к другому участку молекулы эластазы 1 во время следующей инкубации. К
биотиновому участку, в свою очередь, присоединяется метка с красителем. Степень
интенсивности окраски, которую определяют спектрофотометрически, указывает на
количество эластазы 1 в образцах. Таким образом, можно говорить о высокой
специфичности данного метода. Возможность определения неинвазивным способом
эластазы 1 путем исследования ее в стуле придает ему еще больше ценности и
значимости, особенно в педиатрии.
Для успешной своевременной диагностики патологии поджелудочной
железы при муковисцидозе необходимо использовать целый комплекс исследований,
включающий наряду с тщательными клиническими наблюдениями за больным ребенком
ряд функциональных и инструментальных методов, позволяющих наиболее полно
изучить степень поражения поджелудочной железы с целью назначения адекватной
комплексной терапии. Метод ультразвуковой диагностики с допплерографией и
определение фермента эластазы-1 в кале характеризуются безопасностью,
неинвазивностью, возможностью применения в динамике, графической регистрацией
полученных данных, общедоступностью.
Результаты собственных исследований
Нами обследовано 32 ребенка в возрасте от 6 месяцев до
17 лет. Диагноз установлен в возрасте от 1 месяца до 14 лет. Генетическое
обследование было проведено 26 больным. У всех обследованных детей была
смешанная форма заболевания. Первые проявления кишечного синдрома у больных МВ
определялись в виде учащенного разжиженного «жирного» стула у 18 больных,
появления периодических болей в животе у 2 больных, запоров у 3 больных. У 11
детей выраженных жалоб со стороны желудочно-кишечного тракта родители не
предъявляли, однако при углубленном обследовании данных больных были выявлены
изменения поджелудочной железы. У 19 детей кишечный синдром проявился с
рождения. Отставание в физическом развитии было выявлено у 28 детей по массе и
у 15 больных по росту.
Всем детям проводили комплексное клинико-лабораторное
и инструментальное обследование, включающее общий анализ крови и мочи,
копрограмму, посев мокроты на микрофлору и чувствительность к антибиотикам,
рентгенографию органов грудной клетки и пазух носа, исследование функции
внешнего дыхания, электрокардиографию, генетическое обследование,
ультразвуковое обследование с допплерографией органов брюшной полости. Диагноз муковисцидоз
у больных детей неоднократно подтверждался положительным потовым тестом c
помощью тест системы Macroduct. Дополнительно проводился тест определения
фермента поджелудочной железы эластазы 1 в кале для выявления панкреатической
недостаточности у больных
муковисцидозом методом ИФА диагностики. Данный метод является «золотым
стандартом» в диагностике панкреатита, который объективно отражает степень
недостаточности экзокринной функции поджелудочной железы, на показатели
которого не влияет проводимая заместительная терапия панкреатическими
ферментами, а также является простым, точным, не прямым и неинвазивным методом
определения панкреатической недостаточности у детей больных муковисцидозом.
По данным Н.Ю. Каширской и соавт., панкреатическую
недостаточность имеют около 85% больных муковисцидозом (МВ). Она проявляется в
основном в нарушении ассимиляции жира и стеатореи той или иной степени.
Остальные 10-15% больных составляют группу с относительно сохранной функцией
поджелудочной железы (ПЖ) без нарушения усвоения жира. Однако, если тщательно
исследовать ее функцию у этих больных, то и у них обнаруживаются значительные
отклонения от нормы. Выявлено, что у большинства пациентов с клинически
сохранной функцией ПЖ уровень липазы колеблется в пределах нижней границы или
даже ниже нормы. Установлено, что для предотвращения мальдигестии достаточно
секреции всего от 1 до 2% общей липазы и колипазы. Таким образом, у 85% детей с
клинически выраженной панкреатической недостаточностью потеря экзокринной
функции составляет 98-99% [11].
В исследуемую группу вошло 34 ребенка с
муковисцидозом. По уровню эластазы 1 в кале больных МВ разделили на 3 группы: В
1 группу вошли дети с выраженным снижением фекальной эластазы 1 (менее 100
мкг/г), во 2 группу дети с умеренным снижением данного фермента (100–200
мкг/г). В 3 группе у детей с нормальными значениями Эластазы-1 (200–10000
мкг/г) отмечались признаки синдрома мальабсорбции, что, видимо, можно объяснить
сочетанной патологией ПЖ и гепатобилиарной системы либо предположить недостаточную
чувствительность эластазы 1 для легкой степени панкреатической недостаточности
(рис.4.1).
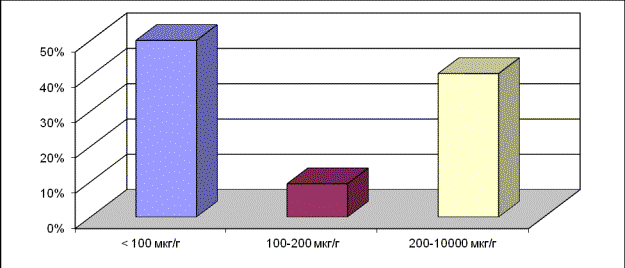
Рис.4.1. Распределение больных муковисцидозом в
зависимости от показателей эластазы 1 в стуле
Всем детям проводили ультразвуковое обследование
поджелудочной железы с допплерографией (табл.4.1). Ультразвуковое исследование
проводилось у детей 7–17 лет утром натощак на ультразвуковом сканере Toshiba Xario
конвексным датчиком частотой 3,5 МГц в реальном масштабе времени в В-режиме.
Определялись размеры, эхогенность, контуры, поджелудочной железы, форма,
поперечные размеры головки, тела и хвоста ПЖ, изменение эхогенности, изменение
эхоструктуры, контуры, подвижность органа, а также диаметр, линейная скорость
кровотока и объемная скорость кровотока в селезеночной вене. Данные параметры
также оценивались постпрандиально.
Выявлена четкая зависимость между показателями
эластазы 1 в стуле и ультразвуковыми показателями поджелудочной железы.
Таблица 4.1
Изменение ультразвуковых
характеристик поджелудочной железы у детей с муковисцидозом
|
Критерии |
Муковисцидоз . Хроническая панкреатическая недостаточность. n=27 (%) |
|
Увеличение
размеров одного или всех отделов ПЖ Уменьшение
размеров одного или всех отделов ПЖ |
14 (51,8%) 8 (29,6%) |
|
Изменение эхогенности: - повышение |
20 (74%) |
|
Изменение эхоструктуры: -
гиперэхогенные включения |
12 (44,4%) |
|
Контуры
ПЖ: -
четкие -нечеткие |
9 (33,3%) 23 (85,1%) |
|
Подвижность
ПЖ -сохранена -снижена |
12 (48,1%) 22 (81,5%) |
|
Диаметр
селезеночной вены: -норма -увеличен |
13 (48,1%) 14 (51,8%) |
|
Кровоток
селезеночной вены: -линейная
скорость: снижена норма увеличена -объемная
скорость: снижена норма увеличена |
10 (37%) 4 (14,8%) 13 (48,1%) 8 (29,6%) 5 (18,5%) 10 (37%) |
Установлено, что у большинства детей с МВ отмечается
повышение эхогенности ПЖ, контуры нечеткие и неровные, снижена подвижность
органа, что косвенно может говорить о фиброзных изменения в ПЖ.
Дополнительно к общепринятой ультразвуковой методике
проводилась допплерография с постпрандиальная оценкой кровотока селезеночной
вены (СВ). Г.И. Кунцевич с сотрудниками проводили оценку кровотока в СВ у
взрослых здоровых лиц до и после приема пищи и установили, что в селезеночной
вене уже через 5-10 мин после приема пищи происходит прирост линейной скорости
кровотока на 70% Параллельно с этим регистрируется увеличение объёмной скорости
кровотока, достигающей максимального прироста на 110-120% через 40 мин [13].
Исследование кровотока в СВ является более
информативным и дает более раннюю характеристику функционального состояния
поджелудочной железы, что способствует ранней диагностике и прогнозированию
течения заболевания. Определялся диаметр СВ, проводилась PW-импульсная допплерография, которая включала измерение
скорости линейного кровотока (СЛК) и объёмной скорости кровотока (ОСК) в СВ.
После этого ребенок получал физиологический завтрак. Спустя 40 мин определялись
размеры поджелудочной железы, диаметр, скорость линейного кровотока (СЛК) и
объёмная скорость кровотока (ОСК) в СВ (рис. 4.2, 4.3). Исследование больных
проводили в положении лежа на спине, левом и правом боку. Датчик размещали в
эпигастральной области, правом и левом подреберьях. Во всех случаях проводили
исследование не только ПЖ, но и печени, селезенки, желчного пузыря, а также
сосудов систем воротной и нижней полой вен. При этом изучались форма, размеры,
структура печени и селезенки.
Нами выявлена сильная взаимосвязь между ОСК натощак и
постпрандально (r = 0,79; p = 0,01) и ЛСК
натощак и постпрандиально (r = 0,51; p =
0,05).
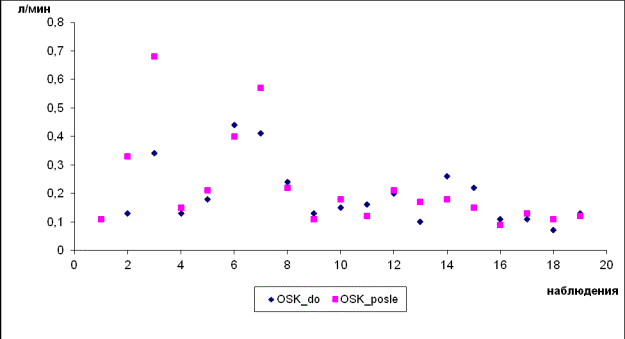
Рис. 4.2.
Показатели ОСК натощак и постпрандиально
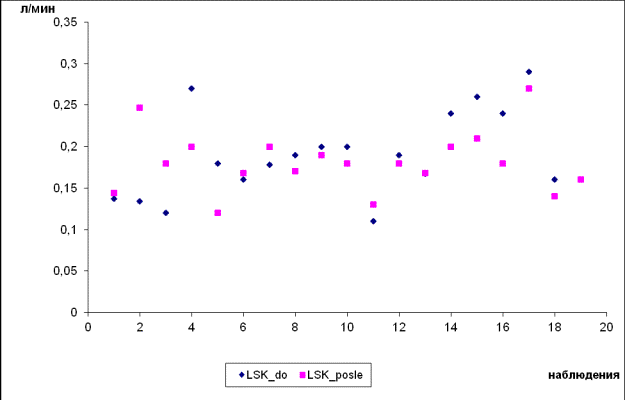
Рис. 4.3.
Показатели ЛСК натощак и постпрандиально
Выявлена взаимосвязь снижения уровня фекальной
Эластазы и изменения диаметра СВ (r = 0,59; p = 0,01). Таким образом, состояние кровотока в СВ
имеет важное диагностическое значение так как может быть использовано для
ранней оценки функционального состояния поджелудочной железы.
Клинические примеры.
Пример 1. Мальчик 8 лет.
Поступил с жалобами на затруднение носового
дыхания, малопродуктивный кашель с отхождением густой, вязкой мокроты.
Анамнез заболевания: с рождения у ребенка отмечается плохая прибавка в массе,
персистирующий респираторный синдром, полифекалия, стеаторея, креаторея. С
раннего возраста состоит на «Д» учете с диагнозом муковисцидоз, диагноз
подтвержден положительным потовым тестом. В 2006 г/ генетическое тестирование в
лаборатории НИИ АиГ им. Д.Отта: гомозиготен по мутации DEL F 508. Находится на
заместительной терапии «Креоном» – 25000 ЕД липазы на прием пищи, 10000 на
перекус. Инвалид детства. В посевах мокроты Ps.aeruginosae. Течение заболевания тяжелое. Частые обострения
бронхолегочного процесса, формирование хронического синусита, наличие признаков
хронической панкреатической недостаточности.
Объективно:
общее состояние тяжелое по заболеванию, за счет респираторного синдрома,
хронической панкреатической недостаточности, хронической гипоксии, хронической
интоксикации. Телосложение правильное. Самочувствие удовлетворительное. Масса
долженствующая 22 кг, масса фактическая 21 кг, рост долженствующий 116 см, рост
фактический 115 см, физ. развитие соответствует возрасту. Кожа и видимые
слизистые бледные суховатые. Периферические л/у не увеличены. Кашель
малопродуктивный влажный, мокроту не выплевывает. Грудная клетка визуально
цилиндрическая, со склонностью к эмфизематозному вздутию, в акте дыхания
участвует симметрично, дыхание без участия вспомогательной мускулатуры.
Экскурсия грудной клетки не нарушена. Тип дыхания грудной. ЧДД 20 в мин. ОГР
клетки 65 см, одышки нет. Грудная клетка эластичной консистенции, пальпация
безболезненна. Перкуторный звук с коробочным оттенком. Хрипы непостоянные
влажные среднепузырчатые на вдохе с
обеих сторон. Признаки хронической гипоксии в виде «часовых стекол» и
«барабанных палочек». Дыхание затруднено, выделения слизисто-гнойные. Живот
мягкий, увеличен в объеме за счет расширенных петель кишечника, метеоризма,
болезненность в области эпигастрия, желчно-пузырные симптомы положительны.
Печень +1 см из-под края реберной дуги. Стул оформленный 1–2 раза в день,
видимой стеатореи нет. Положительный симптом Мейо-Робсона.
Лабораторно-инструментальные данные: липаза крови 1,9 Е/л (N 60–190 Е/л), амилаза крови
39,6 Е/л (до 200 Е/л), эластаза 1 в кале 21,7 мкг/г (N 200–10000 мкг/г). Копрограмма: стеатореи, креатореи нет (на фоне
заместительной терапии Креоном).
УЗИ с
допплерографией:
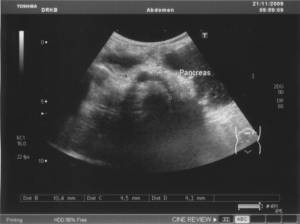

Рис. 4.4. Хронический панкреатит у ребенка 8 лет.
Эхогенность паренхимы поджелудочной железы повышена в значительной степени
Ультразвуковое исследование проводится утром, натощак.
Поджелудочная железа, размеры натощак: головка 9,8 мм,
тело 6,9 мм, хвост 7,2 мм, гиперэхогенная, контуры нечеткие, гиперэхогенные
включения 1,4 мм (кисты?). Диаметр селезеночной вены 5,5 мм, скорость линейного
кровотока 0,19 м/сек, объёмная скорость кровотока 0,24 л/мин.
Поджелудочная железа постпрандиально: головка 10,4 мм,
тело 9,5 мм., хвост 9,2 мм. Диаметр селезеночной вены 3,8 мм, скорость
линейного кровотока 0,17 м/сек , объёмная скорость кровотока 0,22 л/мин.
Заключение:
отмечается уменьшение размеров поджелудочной железы натощак (норма по
Дворяковскому в 7–9 лет: головка 16 мм, тело13 мм, хвост 13 мм). Неоднородная,
наличие кист. Диаметр СВ уменьшен. ЛСК и ОСК снижена.
Диагноз:
Муковисцидоз, смешанной формы, тяжелое течение. Хроническая пневмония с
явлениями распространенной деформации бронхов, бронхоэктазами, период
обострения. ДН 1 ст. хронический риносинусит, период обострения. Хроническая
панкреатическая недостаточность.
Генетический диагноз: носитель мутации DEL F 508 в
гомозиготном положении. МАРС (ДЛХЖ, ПМК 1 ст. без регургитации).
Пример 2.
Пациент 16 лет.
Жалобы при поступлении на субфебрилитет, влажный кашель с отхождением
скудной гнойной мокроты зеленого цвета, заложенность носа.
Анамнез заболевания: ребенок впервые госпитализирован в реанимационное
отделение в возрасте 2 месяцев с диагнозом пневмония, где находился на ИВЛ. Пневмония
протекала с признаками обструктивного синдрома, ателектазами. Со стороны
кишечника отмечалась полифекалия и метеоризм. С рождения мама отмечала жирный
стул. С 3 месяцев до 9 месяцев периодически находился на стационарном лечении с
диагнозом: Очагово-сливная пневмония. ВПС (ДМПП). В 9 месяцев выставлен
диагноз: Муковисцидоз смешанная форма, тяжелое течение. ВПС. При госпитализации
в пульмонологическое отделении проведено определение хлоридов пота – 114
мкмоль/л. Ребенок находится постоянно на заместительной терапии «Креоном»,
муколитической терапии. В 2006 году проведено молекулярно-генетическое
обследование, выявлена мутация 2143 del
трансмембранного регуляторного белка муковисцидоза. В 2003 году
остеобластокластома левой плечевой кости, в 2005 г. проведена операция.
Анамнез жизни: ребенок от 3 беременности 2 родов, беременность на
фоне раннего токсикоза. Масса при рождении 3000 г, рост 53 см. Находился на
грудном вскармливании до 1 месяца, затем смешанное, с 3-х месяцев
искусственное.
Первый ребенок в семье здоров.
Перенесенные заболевания: ОРЗ, ветряная оспа, краснуха. Гемотрансфузии были.
Объективно:
состояние ребенка тяжелое за счет респираторного синдрома, хронической
панкреатической недостаточности, хронической гипоксии, хронической интоксикации.
Самочувствие не нарушено, мальчик активный. Сон и
аппетит не нарушены, астеническое телосложение. Кожные покровы бледно-розового
цвета, умеренно влажные. Язык влажный, не обложен. Зев спокойный. Имеются
признаки хронической гипоксии в виде «барабанных палочек» и «часовых стекол».
Подкожно-жировая клетчатка развита слабо, распределена не равномерно. Масса
фактическая 38 кг, рост фактический 163 см. Л/у не увеличены. Носовое дыхание
затруднено преимущественно справа. Отмечается гнусавость голоса. Объем грудной
клетки на вдохе 69 см, на выдохе 66 см, экскурсия грудной клетки 3 см. При
аускультации выслушивается везикулярное дыхание, хрипы не слышу. При перкуссии
коробочный звук. Тоны сердца ясные, сердцебиение ритмичное.
Живот мягкий безболезненный при пальпации, участвует в
акте дыхания. Отмечается болезненность в точке Кача.
Печень +1 см из под - края реберной дуги. Селезенка не
увеличена.
Стул оформленный 2
раза в день, видимой стеатореи нет.
Диурез адекватный.
Лабораторно-инструментальные данные: амилаза крови 54,9 Е/л (N до 200 Е/л), эластаза 1 в
кале 37,2 мкг/г (N 200–10000 мкг/г); копрограмма: стеаторея +, креаторея + (на
фоне заместительной терапии «Креоном»).
УЗИ с
допплерографией:


Рис. 4.5. Хронический панкреатит у ребенка 16 лет.
Гиперэхогенные включения (кисты 2×3 мм). Эхогенность паренхимы
поджелудочной железы повышена в значительной степени
Ультразвуковое исследование проводится утром, натощак.
Поджелудочная железа размеры натощак: головка 14,9 мм,
тело 16,1 мм, хвост 13,4 мм., гиперэхогенная, контуры нечеткие, гиперэхогенные
включения 2×3 мм (кисты). Диаметр селезеночной вены 4,4 мм, скорость
линейного кровотока 0,20 м/сек, объёмная скорость кровотока 0,15 л/мин.
Поджелудочная железа постпрандиально: головка 16,3 мм,
тело 13,7 мм, хвост 11,4 мм. Диаметр селезеночной вены 4,8 мм, скорость линейного кровотока 0,18 м/сек,
объёмная скорость кровотока 0,18 л/мин.
Заключение:
размеры поджелудочной железы не увеличены. Кисты размером 2×3 мм. Диаметр
СВ уменьшен, ЛСК и ОСК снижены.
Диагноз:
Муковисцидоз, смешанная форма, тяжелое течение. Бронхоэктазы в S 2, 3, 4, 5, 6,
8, 9, 10 справа, S 1, 2, 4, 5, 9, 10 слева. Хроническое носительство Pseudomonas
aeruginosa. Хронический гайморит. Хроническая панкреатическая недостаточность.
Отставание в физическом развитии.
Пример 3. Девочка 6 лет.
Поступила с жалобами на влажный кашель с
выделением гнойной мокроты в небольшом количестве, одышку, отсутствие аппетита,
субфебрильную температуру.
Анамнез заболевания: больна с рождения, родилась с массой тела 3320 г, в
первые месяцы жизни – частый жирный стул со зловонным запахом, плохая прибавка
в массе тела несмотря на хороший аппетит. 1,5 мес – респираторный синдром в
виде навязчивого приступообразного кашля.
Перенесённые заболевания: бронхиты, пневмонии,
постоянный кашель с гнойной мокротой. Диагноз выставлен в августе 2004 г.,
подтверждён положительным потовым тестом (хлориды пота 108 – 100 ммоль/л).
Получает постоянно заместительную терапию ферментными препаратами, в настоящее
время –«Креон» 25000 ЕД на основной прием пищи, 10000 на перекус, видимой
стеатореи, полифекалии нет.
Анамнез жизни:
ребенок от II беременности, протекавшей на
фоне токсикоза на поздних сроках, I срочных
родов путем кесарева сечения. Масса при рождении 3320 г, рост 50 см. Выписана
из РД на 5 сутки, БЦЖ в РД.
Аллергологический анамнез не
отягощен, гемотрансфузии не было.
Объективно:
состояние тяжелое за счет хронической гипоксии, хронической панкреатической
недостаточности. Одышка не выражена. Положение активное. Сознание ясное. Физическое развитие: масса 14 кг (II), длина тела 108 см (VI), дефицит массы тела 2 ст.
Кожа чистая. Видимые слизистые влажные,
чистые. Акроцианоз, цианоз носа при нагрузке. Носовое дыхание свободное.
Периферические лимфатические узлы не увеличены. Грудная клетка эмфизематозно
вздута. Над легкими перкуторный звук с коробочным оттенком, аускультативно
дыхание одинаково с обеих сторон, хрипов нет. Тоны сердца ясные, систолический
шум на верхушке. Живот мягкий, увеличен за счет гипотонии, метеоризма. Печень
+1,5–2 см. Полифекалии, видимой стеатореи нет.
Лабораторно-инструментальные данные: липаза крови 12,7 Е/л (N 60–190 Е/л, амилаза крови 51,1 Е/л (N до 200 Е/л), эластаза-1 в кале 48,9 мкг/г (N 200–10000 мкг/г). Копрограмма:
нейтральный жир «+» на фоне заместительной терапии «Креоном».
УЗИ с допплерографией:

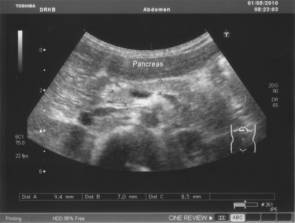
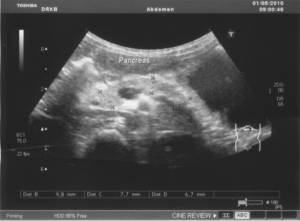
Рис.4.6. Эхограмма поджелудочной железы ребенка 6 лет.
Значительное повышение эхогенности поджелудочной железы. Контуры нечеткие,
неровные
Ультразвуковое исследование проводится утром, натощак.
Поджелудочная железа размеры натощак: головка 9,4 мм,
тело 7,0 мм, хвост 6,5 мм., гиперэхогенная, контуры нечеткие, неоднородная с
гиперэхогенными участками в области тела и хвоста (кисты?). Диаметр селезеночной
вены 3,2 мм, скорость линейного
кровотока 0,27 м/сек, объёмная скорость кровотока 0,12 л/мин.
Поджелудочная железа постпрандиально: головка 9,8 мм.,
тело 7,7 мм., хвост 6,7 мм. Диаметр селезеночной вены 3,4 мм, скорость линейного кровотока 0,33 м/сек,
объёмная скорость кровотока 0,17 л/мин.
Заключение:
размеры поджелудочной железы уменьшеумны, кисты в области тела и хвоста.
Диаметр СВ уменьшен, ЛСК и ОСК снижены.
Диагноз: Муковисцидоз, смешанная
форма, тяжелое течение. Вторичная пневмония с явлениями деформирующего
бронхита, бронхоэктазами, пневмосклерозом, период обострения. ДН II.
Хронический высев из мокроты Ps.aeruginosa. Хроническая
панкреатическая недостаточность. Отставание в физическом развитии, дефицит
массы тела II ст. МАРС: ДХЛЖ. ООО 4,3 мм. Вторичная легочная
гипертензия. Анемия легкой степени, смешанной этиологии. Правосторонний
катаральный гайморит. Аденоиды I – II ст., обострение. Хр.
периодонтит.
Таким
образом, только комплексная оценка
поджелудочной железы у детей с муковисцидозом может дать полное
представление о функциональном и структурном состоянии данного органа. Такие
неинвазивные методы, как ультразвуковая диагностика с использованием
допплерографии и определение фермента эластазы 1 в кале, помогут
врачам-клиницистам выявить ранние изменения со стороны ПЖ и разработать тактику
дальнейшего ведения с учетом полученных результатов.
ЛИТЕРАТУРА
1. Корниенко Е.А. Внешнесекреторная
функция поджелудочной железы у детей с заболеваниями органов пищеварения. /
Ю.И. Постникова, Т.Б. Лобода, С.А. Фадина.
Независимое издание для практикующих врачей. – Москва, 2007.
2. Аряев Н.Л. Муковисцидоз у детей. // Е.А.
Старец Киев, 2004.
3. Пыков М.И. Детская ультразвуковая
диагностика М 2001 .
4. Дворяковский И.В. Новые возможности
ультразвуковых исследований органов брюшной полости при муковисцидозе у детей.
/ О.И. Симонова, Г.М. Дворяковская, М.О. Горбунова // Российский педиатрический
журнал. №4–2008г.
5. Охлабыстин А.В. Муковисцидоз:
современные возможности диагностики и лечения. // Жур. Гастроэнтерология №2. С.
53–56.
6. Коровина Н.А.. Экзокринная
недостаточность поджелудочной железы: проблемы и решения. / И.Н. Захарова, Н.Е.
Малова. // Рук.для врачей, – Ч III. – М. – 2004.
7. Хендерсон Д.М. Патофизиология органов
пищеварения. // – М. – 1997 г.
8. Коровина Н.А. Экзокринная
недостаточность поджелудочной железы. / И.Н. Захарова, Н.Е. Малова // Вопросы
современной педиатрии,., – Т.2, – №5. – 2003.
9.
Бельмер С.В. Экзокринная недостаточность поджелудочной железы у детей: методы
диагностики и коррекции (методические аспекты) / Т.В. Гасилина //— М., — С. 12.
– 2001. .
10.
Капранов Н.И. Муковисцидоз (Современные достижения и проблемы) / Л.А. Шабалова,
Н.Ю. Каширская. // Методические рекомендации. — М.: Медпрактика, 2001. — 76.
11.
Каширсая Н.Ю. Диагностическое значение непрямого метода определения
панкреатической недостаточности эластазы-1 в стуле у больных муковисцидозом. /
Н.И Капранов, Н.Ф Кабанова., Е.А. Калашникова // Пульмонология. – 2001. –
Vol.11, №3, С 57-60.
12.
Римарчук Г.В. Постпрандиальная
ультразвуковая оценка поджелудочной железы / С.И. Полякова, А.В. Лебедева. //
Рос.жур.гастроэнтерологии, гепатологии, колопроктологии. – 1999. – Т IX. – №5.
– С.79.
13. Кунцевич Г.И. Оценка состояния
портального кровообращения у больных циррозом печени по данным дуплексного
сканирования. // Визуализация в клинике. - 1994, -№5 - С.33-38
14. Успенский Ю.П. Функциональная
диагностика в гастроэнтерологии / В.А. Ратников. // Учебно-методическое
пособие. Санкт-Петербург – 2002. –С 61-62.
15. Григорьев П.Я. Сравнительная оценка методов
диагностики нарушений внешнесекреторной функции поджелудочной железы. / Э.П. Яковенко,. А.Д. Дибиров, О.В. Бочкарев // – М, –2005.
16. Ebbehoj N. Evalution of
pancreatic tissue fluid pressure and pain in chronic pancreatitis – A
longitudinal study. / L. Borly, J. Bulow, J. Scand. // Gastroenterology., 1990;
25: 462–466.
17
Friess H. Enzyme treatment after gastrointestinal surgery. / J. Bohm, M.Ebert
// Digestion, 1993, 54 (suppl.2). 48–53.
17. Jhee I. Pancreatic pain: Is
there a medical alternative to surgery? / R. Andersson, J. Axelson. //
Digestion, 1993; 54 (suppl 2): 30–34
19 Mc
Mahon M.J.. Acute pancreatitis: When is enzyme treatment inducated. Digestion // 1993; 54 (suppl2): 40–42.