Химия и химические технологии / 8. Кинетика и катализ
Д.х.н. 1Чурина
Д.Х., к.х.н.1Ергазиева Г.Е., д.т.н. 2Тургумбаева Р.Х., 2Жамигат
М., 1Ахмет О.
1Институт проблем
горения
2Казахский национальный
педагогический университет им. Абая
Влияние носителей на активность
кобальтовых катализаторов в синтезе
Фишера-Тропша
С уменьшением запасов
нефти использование альтернативных источников получения различных видов
топлива, углеводородов и других важных для промышленности продуктов из
синтез-газа (синтез Фишера-Тропша - СФТ),
природного газа, угля, биомассы и другого ненефтяного сырья становится
актуальным и имеет перспективу для Казахстана.
Синтез-газ,
представляющий собой смесь оксида углерода и водорода в различных соотношениях,
легко может быть получен как из угля, биомассы, так и из любого другого
углеродсодержащего сырья. Синтез Фишера - Тропша (СФТ) протекает с
участием катализаторов [1-4], которые представляют собой сложные системы,
включающие активный компонент из металлов VIII группы, промотор и носитель. В качестве активного
компонента катализатора в основном используют кобальт или железо [5].
Кобальтовые системы по сравнению с железом отличаются большей гидрирующей
активностью и инертностью в реакции водяного газа. Кроме того, катализаторы на
основе кобальта характеризуются большей стабильностью [6].
Состав конечных продуктов синтеза Фишера-Тропша зависит от катализатора, температуры
процесса и соотношения СО и Н2. Так, на металлоокисном катализаторе
получают метанол с примесью этанола и диметилового эфира [7]. Это основной
процесс получения метанола в мире, обычная мощность метанольных заводов
составляет около 0,5 млн. т в год (Новомосковское ПО «АЗОТ»; кобальтовый
катализатор).
Для производства
моторных топлив метанол перерабатывается в диметиловый эфир и далее
в смесь разветвленных предельных углеводородов (процесс Mobil GTG в Мауи, Новая
Зеландия; кобальтовый катализатор) [8]. На кобальтово-цинковых катализаторах,
характеризующихся гидрирующей активностью, получают смесь линейных алканов
(процесс AGC-211 в Бинтулу, Малайзия) [9].
На железном катализаторе получают смесь линейных и разветвленных алканов
и алкенов (перспективный процесс Рентех).
На кобальтовых или
родиевых катализаторах при давлении выше 10 МПа и температуре в диапазоне
140-180°С алкены взаимодействуют с синтез-газом и превращаются в альдегиды -
важнейшие полупродукты в производстве спиртов, карбоновых кислот, аминов,
многоатомных спиртов и др. Мировое производство альдегидов по такой технологии
(оксосинтез) достигает 7 млн т в год [10]. Одно из важных современных
направлений научного поиска в области синтеза Фишера- Тропша состоит в
получении кислородсодержащих продуктов. Введение таких соединений в количестве
1 % в дизельное топливо снижает содержание сажи в продуктах сгорания на 4 –
10%.
Катализатор для синтеза
углеводородов из синтез-газа [11] содержит от 2 до 50% кобальта и от 0,1 до 15%
магния или смеси магния и циркония, находящихся на подложке из диоксида титана.
Изобретение находит применение в синтезе углеводородов, в частности воска, с
использованием синтеза по Фишеру-Тропшу. Процесс отличается высокой
эффективностью, а также - пропускной способностью каталитического процесса.
Существуют важные
стимулы для применения способа превращения угля в жидкое топливо и для превращения
природного газа в жидкое топливо. Жидкое топливо легче транспортировать и
использовать, чем уголь. Превращение природного газа в жидкий делает
транспортировку и хранение более удобными. Sasol в Южной Африке эксплуатирует
коммерческие заводы, работающие на основе синтеза по Фишеру-Тропшу, на которых
используют железный катализатор [12]. Запущено производство на большом
коммерческом заводе в Малайзии, на котором используют технологию получения
масел Shell. В указанных коммерческих производствах обычно используют системы
реакторов с неподвижным слоем; например, превращение природного газа в
транспортное топливо посредством способа синтеза среднего дистиллята фирмы
Shell согласно [13].
В принципе все
катализаторы, которые являются активными в случае синтеза по Фишеру-Тропшу,
можно использовать в системах суспензионных реакторов. Целью выбора
катализатора является получение наиболее высокой возможной избирательности
требуемых жидких углеводородных продуктов и самой высокой возможной активности.
Железные катализаторы предпочтительны вследствие низкой стоимости и хорошей
активности. Однако имеются лучшие системы катализатор - реактор, например,
катализатор на основе кобальт-марганцевой шпинели, активируемый медью [11].
Обычными катализаторами
для синтеза по Фишеру-Тропшу являются кобальт и железо [13]. Другие металлы
группы VIII, такие как рутений и осмий, также активны. В качестве основных
компонентов катализатора исследованы металлы, включающие рений, молибден и
хром, но они обладали очень низкой активностью или были неактивны и производили
главным образом метан. Активность кобальтовых катализаторов на подложках может
быть усилена или может быть модифицирована добавлением различных металлов,
таких как медь, церий, рений и марганец, либо драгоценных металлов, включающих
платину, иридий, рутений и родий [11]. Помимо усиления активности катализатора,
промоторы добавляют для того, чтобы достичь конкретных результатов, например,
чтобы повысить производство жидких углеводородов, чтобы подавить получение
метана. Так, описан катализатор, содержащий кобальт и один дополнительный
элемент (молибден или вольфрам), и по меньшей мере один из элементов,
включающих рутений и медь [11].
Каталитической
переработке синтез-газа посвящено большое количество исследований. Компания
BASF запатентовала процесс получения смесей углеводородов и спиртов из
синтез-газа над подщелоченными Co-Os катализаторами. К 1945 г. в мире
(Германия, США, Китай, Япония) насчитывалось 15 заводов, производящих синтез
жидких углеводородов из синтез - газа на металлических (Со, Ni, Fe)
катализаторах. Наиболее распространенными носителями для кобальтовых
катализаторов синтеза жидких углеводородов из СО и Н2 являются
силикагель, оксиды алюминия и титана. Синтез-газ, богатый водородом,
способствует образованию парафинов [14].
Целью настоящей работы было исследование
влияния носителей на активность кобальтовых катализаторов в реакции
Фишера-Тропша. В качестве носителей для катализаторов синтеза Фишера-Тропша
были изучены оксиды металлов и цеолиты.
Методика
эксперимента
Эксперименты по испытанию каталитической
активности нанесенных на различные
носители катализаторов проводились на проточной каталитической установке
(рисунок 1). Продукты реакции идентифицировались хроматографически на приборе "ХРОМОС ГХ-1000" с использованием
метода абсолютной калибровки и детекторов по теплопроводности. Разделение
компонентов проводилось на колонках (длина 2 м, внутренний диаметр 3 мм),
заполненных цеолитом NaX и порапаком-Т, газы - носители - гелий и аргон.

Рисунок 1 - Проточная
каталитическая установка
Катализаторы были приготовлены методом
нанесения предшественника активного компонента - водного раствора азотнокислой
соли кобальта на носители путем пропитки по влагопоглощению. Термообработка
катализаторов проводилась при температурах 400-500оС в течение 3
часов. Катализаторы перед началом опыта восстанавливались в токе водорода.
Результаты и обсуждение
Влияние природы носителя на активность нанесенных
катализаторов является одним из важных аспектов гетерогенного катализа. В
процессах Фишера-Тропша эта проблема рассматривается в ряде работ [15-17].
Предполагается, что природа носителя влияет на изменение валентного и
координационного состояния металла, его окислительно-восстановительного потенциала. Среди большого разнообразия
носителей оксид алюминия и оксид кремния являются наиболее доступными и
относительно недорогими носителями катализаторов, однако наряду с ними
используют ряд других носителей [18-19].
Нами в качестве носителей
для катализаторов синтеза Фишера-Тропша
(СФТ) были исследованы оксид алюминия гамма модификации, оксид кремния и
цеолиты: γ–Al2O3, SiO2, KA, NaА, CaA и NaХ. Носители были
изучены при условиях реакции: W=1500 ч-1, Тр=200-500оС. Для гидрирования
оксида углерода была использована модельная смесь с соотношением Н2/СО=2.
На исследуемые носители был нанесен оксид кобальта концентрации 3 мас. %.
На рисунке 2
представлены результаты влияния природы носителей на активность оксида кобальта
в гидрировании оксида углерода. Как видно из рисунка 2, с нанесением оксида кобальта на цеолиты KA и CaA наблюдается
очень низкая конверсия оксида углерода, тогда как на цеолитах NaА и NaХ конверсия СО достигает значения 22,0 и 23,1 %,
соответственно.
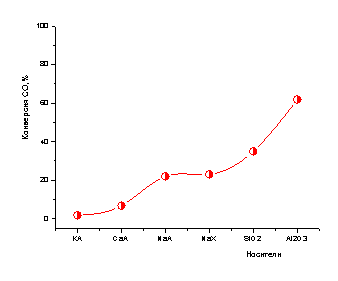
Рис. 2 -
Влияние природы носителя на каталитическую активность оксида кобальта в
конверсии оксида углерода
С нанесением оксида
кобальта на оксидные носители γ–Al2O3 и SiO2 повышается
конверсия оксида углерода. Наибольшая конверсия оксида углерода наблюдается на оксидных носителях: на оксиде алюминия СО (61,9 %), на SiO2
конверсия оксида углерода достигает значения 35 %.
Основными продуктами
синтеза Фишера-Тропша на исследованных носителях являются алканы, узкая фракция
С5-С8 углеводородов и диоксид углерода. В таблице 1
приведены результаты зависимости селективности продуктов реакции от природы
носителей кобальтсодержащего катализатора. Как показывают данные таблицы 1, с
нанесением оксида кобальта на оксидные носители увеличивается гидрирующая
способность катализатора. Основными продуктами реакции являются метан и диоксид
углерода. С нанесением оксида кобальта
на носители NaA и CaA синтезируются жидкие углеводороды, которые на 96 -
100 % состоят из узкой фракции С5-С8 углеводородов.
Наибольшая селективность (43,4 %) по жидким углеводородам наблюдается на Со-катализаторе, нанесенном на носитель CaA.
Таблица 1 - Влияние
активности Со2О3,
нанесенного на различные носители, на селективность продуктов
синтеза Фишера -Тропша
|
Катализатор Со2О3 на носителях |
Селективность по выходу
продуктов, % |
|||
|
SCH4 |
SCO2 |
SC2+ |
SC5-C8 |
|
|
КА |
- |
50 |
- |
- |
|
NaX |
7,0 |
21,9 |
4,3 |
- |
|
NaA |
- |
38,6 |
- |
13,6 |
|
CaA |
2,9 |
21,7 |
7,2 |
43,4 |
|
Al2O3 |
38,8 |
24,7 |
0,2 |
- |
|
SiO2 |
31,4 |
21,4 |
0,9 |
- |
Заключение
В синтезе Фишера - Тропша
исследованы кобальтовые катализаторы, нанесенные на различные носители.
По активности в конверсии
оксида углерода (СО) изученные носители можно расположить в следующем ряду: γ–Al2O3(61,9 %) > SiO2 (35 %)
> NaХ (23,1%) > NaА (22,0%) > CaA (6,9 %) > KA (1,8 %).
По выходу жидких
углеводородов наиболее активными оказались цеолитные носители. Селективность по
С5-С8 углеводородам достигает значения 13,6 % на
кобальтовом катализаторе, нанесенном на носитель NaА и 43,4 % на CaA.
Литература
1. M.E. Dry. The Fischer–Tropsch process: 1950–2000.
// Catal. Today . - 2002.
V. 71. – Р. 227–241.
2. V.R. Pendyala, U.M. Graham, G. Jacobs, H.H. Hamdeh
& B.H. Davis. Fischer-Tropsch synthesis: morphology, phase
transformation, and carbon-layer growth of iron-based catalysts.// ChemCatChem. -2014. V. 6. - Р. 1952–1960.
3. Liu B., Shioyama H., Jiang H., Zhang
X. & Xu. Q. Metal–organic framework (MOF) as a template for
syntheses of nanoporous carbons as electrode materials for supercapacitor // Carbon N.Y.- 2010. V. 48. - P. 456–463.
4. A.J. Amali, J.-K. Sun, & Q.
Xu. From assembled metal-organic framework nanoparticles to hierarchically
porous carbon for electrochemical energy storage // Chem. Comm.- 2014. V. 50. - P. 1519–1522.
5. H.J. Lee, W. Cho, E.
Lim & M. Oh. One-pot synthesis of magnetic particle-embedded
porous carbon composites from metal-organic frameworks and their sorption
properties // Chem. Comm. -2014. V. 50. - P. 5476–5479.
6. J. Gurgul, K. Łątka, I. Hnat, J. Rynkowski
& S. Dzwigaj. Identification of iron species in FeSiBEA by DR
UV–vis, XPS and Mössbauer spectroscopy: Influence of Fe // content. Microporous Mesoporous Mater. -2013.
V. 168. - P. 1-6.
7. Э.А. Караханов.
Синтез-газ как альтернатива нефти. 1. Процесс Фишера-Тропша и оксо-синтез //
Соросовский Образовательный Журнал. 1997. № 6. С. 69.
8. Н.Н. Бобров, И.И.
Боброва, В.А. Собянин // Кинетика и катализ, 1993, т. 34, № 4, С. 257-258.
9. I.I. Bobrova, N.N. Bobrov, A.A. Davydov // Catalysis Today, 1995, v.
24, № 3, Р. 429-439.
10. О.В. Крылов, А.Х.
Мамедов // Успехи химии, 1995, т. 64, № 9, С. 935-959.
11. Катализатор синтеза
углеводородов из синтез-газа, способ получения катализатора.
Пандьюла Сэмьюэль,
Майти Сьюдип, Дасандхи Йогеш Чандра, Мьюкхерджи Сомнатх, Майтра Сандип Кумар.
Патентообладатель(и): Council
of scientific and industrial research.
Заявка: 2005133454/04, 31.03.2003 Дата начала отсчета срока действия патента:
31.03.2003. Дата публикации заявки: 27.04.200
12. Oil and Gas Journal, Jan. 20, 1992, Р. 53.
13. S.T. Sie, et al. // Catalysis Today 8, (1991) (371-394).
14. М.М. Сысоев.
Дипломная работа: Сравнительный анализ: методы получения синтез-газа.
Московская государственная академия тонкой химической технологии им. М.В.
Ломоносова. Москва, 2003 г. BestReferat.ru›referat-119895.html.
15. P. Albers, K. Deller, B.M. Despeyroux, A.
Schäfer & K. Seibold XPS-SIMS study on the surface chemistry
of commercially available activated carbons used as catalyst supports // J. Catal.-1992. V. 133. - P. 467-478.
16. C. Huo, The mechanism of potassium
promoter: enhancing the stability of active surfaces // Ang. Chem. Int. Ed. - 2011. V. 50. - P. 7403–7406.
17. H.M. Torres Galvis & K. P. de Jong.
Catalysts for production of lower olefins from synthesis gas: a review // ACS Catal. - 2013. V. 3. - P. 2130–2149.
18. Thomas O.
Eschemann and Krijn P. de Jong.
Deactivation Behavior of Co/TiO2 Catalysts
during Fischer–Tropsch Synthesis // ACS Catal. - 2015. 5 (6).- Р. 3181–3188.
19. Branislav Todić, Vitaly V. Ordomsky, Nikola M. Nikačević, Andrei Y. Khodakov and Dragomir B. Bukur.
Opportunities for intensification of Fischer–Tropsch synthesis through reduced
formation of methane over cobalt catalysts in microreactors // Catal. Sci. Technol.- 2015. № 5. - Р. 1400-1411.