д.х.н.,профессор
Алдабергенов М.К.1, Жумабаева Д.C.1
д.х.н.,профессор
Балакаева Г.Т.2
1Казахский
Национальный университет имени аль-Фараби, Казахстан
2Казахский
Национальный технический университет имени К.И.Сатпаева, Казахстан
Тополого – термодинамический анализ системы
Li2O-Cu2O-P2O5
В последние годы особое внимание уделяется развитию новых
катодных материалов для высокоэффективных литий-ионных батарей (ЛИБ). Большая часть исследований посвящена катодным материалам для
перезаряжающихся (аккумуляторных) ЛИБ со слоистыми, шпинельными и оливиновыми
кристаллическими структурами. В последнее
время появились работы, в которых активно обсуждаются перспективы применения
соединений фосфата. К примеру, использование LiFePO4
в качестве катодного материала, вместо дорогого LiCoO2 может уменьшить стоимость
батарей от 10 % до 50% . Этот материал дешев, безопасен, имеет высокую
плотность энергии и достаточно привлекателен с точки зрения рабочего напряжения
(3,5 В), но обладает исключительно низкой электронной проводимостью.
Нами предложены литированные фосфаты меди в качестве катодных материалов
для литий-ионных аккумуляторов. По нашим исследованиям удельная емкость
литий-медных фосфатов имеет 234 мАч/г. Исследован процесс получения соединения Li3-хCuxРO4
электрохимическим путем при переменном
токе с использованием различных растворов. Синтезированные фосфаты лития-меди
имеют голубой цвет, устойчивы при комнатной температуре.
В данной работе закономерности
твердофазных превращений компонентов в фосфатных соединениях установлены
триангуляцией системы Li2O-Cu2O-P2O5
термодинамическим методом. Разработанная Курнаковым [1,2] сингулярная триангуляция (метод
сингулярных звезд) многокомпонентных систем дает геометрическое изображение
реакций растворения, соединения, замещения, обмена в тройной системе, позволяет
определить направление реакций, установить природу и характер отдельных фаз в
любой части системы, сделать заключение о характере изучаемой системы в целом.
В системе Li2O-Cu2O-P2O5 установлено образование 37 соединений (табл.), многие
из которых описаны в литературе, а некоторые, например, ряд соединений из Li3-хCuхPO4
прогнозированы нами. С использованием «среднеэлектронной функции Гиббса»
проведена триангуляция системы Li2O-Cu2O-P2O5 (рис.).
Методика триангуляции приведена в [3]. На основании метода ионных инкрементов
[4] рассчитаны для каждого соединения системы энергия Гиббса образования и
«среднеэлектронная функция Гиббса».
Таблица –
Соединения системы Li2O-Cu2O-P2O5
|
№ п.п. |
Соединения |
ΔfGo298, кДж/моль |
_______ ΔGo298, кДж/моль*эл |
|
1. |
Li2O |
-562,1 |
-40,15 |
|
2. |
Cu2O |
-173,2 |
-2,62 |
|
3. |
P2O5 |
-1371,7 |
-19,60 |
|
4. |
LiCu2PO4 |
-1284,1 |
-11,89 |
|
5. |
Li2CuPO4 |
-1553,9 |
-18,95 |
|
6. |
Cu3PO4 |
-876,5 |
-6,54 |
|
7. |
Li3PO4 |
-1893,1 |
-33,81 |
|
8. |
CuPO3 |
-818,5 |
-12,04 |
|
9. |
Li0,1Cu2,9PO4 |
-897,7 |
-6,83 |
|
10. |
Li0,2Cu2,8PO4 |
-928,8 |
-7,21 |
|
11. |
Li0,3Cu2,7PO4 |
-975,8 |
-7,73 |
|
12. |
Li0,4Cu2,6PO4 |
-1026,6 |
-8,31 |
|
13. |
Li0,5Cu2,5PO4 |
-1096,5 |
-8,63 |
|
14. |
Li0,6Cu2,4PO4 |
-1156,4 |
-9,77 |
|
15. |
Li0,7Cu2,3PO4
|
-1189,6 |
-10,27 |
|
16. |
Li0,8Cu2,2PO4 |
-1233,7 |
-10,90 |
|
17. |
Li0,9Cu2,1PO4 |
-1267,2 |
-11,46 |
|
18. |
Li1,1Cu1,9PO4 |
-1302,1 |
-12,35 |
|
19. |
Li1,2Cu1,8PO4 |
-1335,8 |
-12,99 |
|
20. |
Li1,3Cu1,7PO4 |
-1373,7 |
-13,71 |
|
21. |
Li1,4Cu1,6PO4 |
-1408,9 |
-14,44 |
|
22. |
Li1,5Cu1,5PO4 |
-1434,9 |
-15,10 |
|
23. |
Li1,6Cu1,4PO4 |
-1462,4 |
-15,83 |
|
24. |
Li1,7Cu1,3PO4 |
-1490,1 |
-16,59 |
|
25. |
Li1,8Cu1,2PO4 |
-1521,1 |
-17,44 |
|
26. |
Li1,9Cu1,1PO4 |
-1532,8 |
-18,12 |
|
27. |
Li2,1Cu0,9PO4 |
-1597,8 |
-20,12 |
|
28. |
Li2,2Cu0,8PO4 |
-1623,7 |
-21,14 |
|
29. |
Li2,3Cu0,7PO4 |
-1657,3 |
-22,33 |
|
30. |
Li2,4Cu0,6PO4 |
-1683,9 |
-23,52 |
|
31. |
Li2,5Cu0,5PO4 |
-1725,5 |
-25,01 |
|
32. |
Li2,6Cu0,4PO4 |
-1783,6 |
-26,86 |
|
33. |
Li2,7Cu0,3PO4 |
-1800,4 |
-28,22 |
|
34. |
Li2,8Cu0,2PO4 |
-1832,8 |
-29,95 |
|
35. |
Li2,9Cu0,1PO4 |
-1867,7 |
-31,87 |
|
36. |
LiCuO |
|
|
|
37. |
LiPO3 |
-1157,4 |
-27,56 |
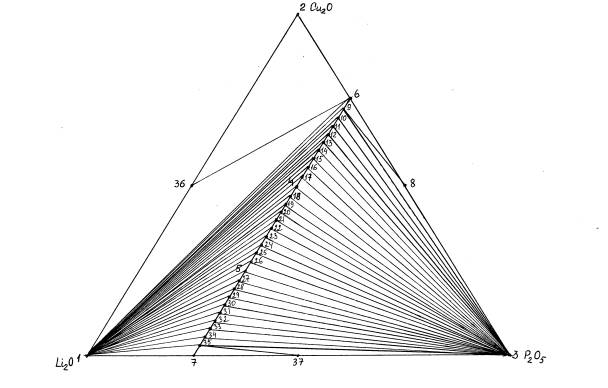
Рисунок –
Триангуляция системы Li2O-Cu2O-P2O5
Триангуляция системы заключается в
разбиении треугольника состава компонентов на вторичные элементы – фазовые
единичные блоки. Фазовый единичный блок (ФЕБ) – это концентрационная область
системы, ограниченная не взаимодействующими между собой индивидуальными
веществами. Совокупность ФЕБов представляет собой триангуляцию системы в
фазовом аспекте.
На
основе триангуляции системы устанавливается фазовый состав продуктов и
химизм протекающих процессов в любой точке системы.
Как видно из рис. для фосфатов меди-лития
наиболее характерны реакции конверсии. Например, конверсия соединения LiCu2PO4 протекает по реакциям: