Хімічні науки / неорганічна хімія
М.Д. Волошин, д.т.н., проф., О.А. Крюковська к.т.н., доцент,
маг. А.Ю.Ружина, маг. Т.М.Бойко
Дніпродзержинський
державний технічний університет (ДДТУ), Україна
Пошук оптимальних умов проведення
електролізу
Під час проведення лабораторних досліджень на сконструйованому лабораторному
електролізері для дослідження технології отримання хлору було відмічено, що
процес електролізу води має змінний характер по часу протікання й об’єму
утвореної суміші газів. Тому метою лабораторних дослідів стало отримання
залежності впливу сили струму, температури електроліту в електролізері, зміни
відстані між катодом і анодом на кількість утворення суміші газів під час
електролізу.
Практично
процес електролізу протікає при високих потенціалах, з перенапруженням.
Перенапруження, тобто різниця між істинним і теоретичним значенням потенціалів
розкладу, залежить від багатьох чинників: матеріалу електрода, щільності
струму, характеру поверхні електрода, температури електроліту. Під час
електролізу хлориду натрію в просторі над залізним катодом виділявся водень,
потенціал розрядження якого більш позитивний, ніж натрію, а в анодному просторі
накопичувався луг. Водночас на графітовому аноді йшов процес виділення хлору,
бо іон ОН- не розряджався внаслідок перенапруження кисню. Таким
чином напрямок процесу в електролізі часто визначається перенапруженням. Сумарно
процес електролізу можна виразити рівнянням:
2NaCl
+ H2O ® 2NaOH +Cl2 +H2
При
цьому хлор може розчинятися в воді з утворенням двох кислот:
Cl2 + H2O ® HClO +HCl
За наявності лугу рівновага легко зсувається праворуч з утворенням NaClO.
Тому необхідно поділяти електролізер на анодний і катодний простір за допомогою
пористої перегородки. На рисунку 1 показано залежність кількості утвореної
суміші газів від зміни відстані між катодом і анодом (зменшення або збільшення
катодного простору), яка отримана лабораторно-практичним шляхом.
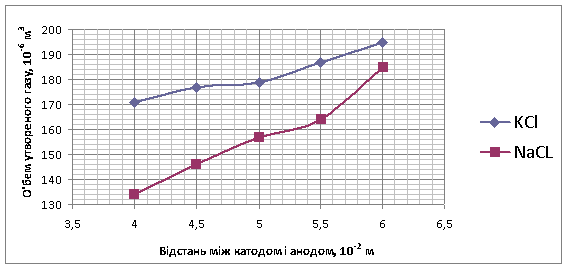
Рисунок 1 – Залежність об’єму
утвореної суміші газів від зміни відстані між катодом і анодом
Концентрація лугу біля катоду збільшувалася по міру протікання процесу, в
той час як концентрація кислоти в анодному просторі була постійною й змінювалася
лише при зміні температури електроліту.
На рисунку 2 наведена залежність об’єму утвореної суміші газів від зміни
температури електроліту.
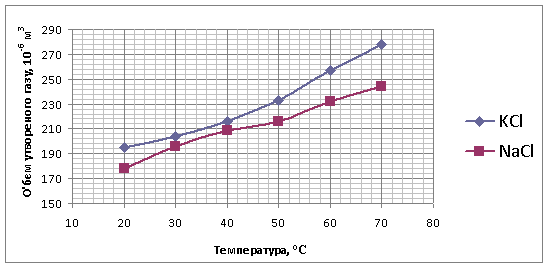
Рисунок 2 – Залежність об’єму
утвореної суміші газів від зміни температури електроліту
Для аналізу
газу, що виділяється з електролізера, використовували апарат Орса. Три
поглинальних судини містять наступні розчини: гіпосульфіт натру (для визначення
хлору), 33% розчин гідроксиду калію (для поглинання СО2) і лужний
розчин пірогалолу (для поглинання кисню). Послідовно визначалися компоненти
газової суміші, поглинаючи спочатку хлор, потім діоксид вуглецю, наприкінці – кисень. Анодний газ із збірки переводили в
судини для визначення хлору і діоксиду вуглецю 6 раз, а в судину для визначення
кисню 12 раз. Після закінчення операції поглинання газів обсяг кожного з них
вимірюють при рівних рівнях рідини в вимірювальній бюретці і зрівнюючій
склянці.
Обсяги утворених
газів обчислювали за наступними формулами.
VCl
= V0 – V1; VCO
= V1 – V2; VO
= V2 – V3
де V0 – обсяг газу взятий на аналіз;
V1 – обсяг газу, що залишався після
поглинання хлору;
V2 – обсяг газу після поглинання
діоксиду вуглецю, що залишався;
V3 – обсяг газу після поглинання кисню,
що залишався.
Вихід хлору по струму
розраховуємо на підставі результатів газового аналізу за формулою
![]()
де: х1, х2 і х3 – вміст в
газі відповідно хлору, діоксиду вуглецю й кисню в перерахунку на безповітряну
суміш, % (об.); х4 – вміст в газі азоту (залишок після аналізу), %
(об.).
Перерахунок
на безповітряну суміш виконують з урахуванням того, що в повітрі на 3.76 обсягу
азоту потрібно 1 обсяг кисню. Тоді значення х1, х2 і х3
можуть бути знайдені наступним чином:
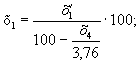
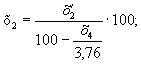
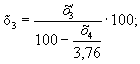
де: х'1,
х'2 і х'3 – вміст
хлору, діоксиду вуглецю і кисню по результатах аналізу, % (об.).
На рисунку 3 наведена залежність об’єму утвореної суміші газів від зміни сили струму.
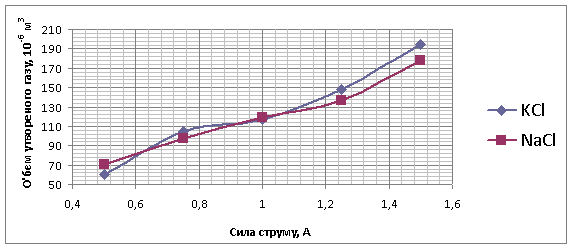
Рисунок 3 – Залежність об’єму утвореної суміші газів від зміни
сили струму
Висновки.
1. Аналіз проведених досліджень показав, що змінюючи температуру
електроліту й силу струму при оптимальному співвідношенні катодного та анодного
простору можливо отримувати необхідну кількість суміші газів оксидантів.
2. Максимальне збільшення виходу суміші оксидантів отримано при збільшенні щільності
струму. Зміна температури розсолу також значно впливає на вихід отриманої
газової суміші. Але великі значення зазначених параметрів негативно впливають
на матеріал електродів, що також потрібно враховувати.
В подальшому планується дослідити вплив оксидантів, отриманих шляхом
електролізу, на кінцевий хімічний склад питної води.
Література
1.
Практикум по прикладной электрохимии: Учебное пособие для вузов
/
Под ред. Н.Т. Кудрявцева. –Л.: Химия,
1980. – 288 с.
2.
Якименко Л.М. Производство водорода, кислорода, хлора и щелочей. - М.:
Химия, 1981. – 280 с.
3.
Б.Б.Дамаскин,
О.А.Петрий, «Введение в электрохимическую кинетику», издательство «Высшая
школа», М., 1983 г.
4.
В.С.Багоцкий,
«Основы электрохимии», издательство «Химия», Л., 1988 г.