Медицина/6. Экспериментальная и клиническая фармакология
Клименко О.В.
Національний медичний університет імені О.О. Боггомольця, Київ,
Україна
ДОСЛІДЖЕННЯ
ЕЛЕКТРОННОЇ ТА ПРОСТОРОВОЇ СТРУКТУРИ МОЛЕКУЛ КАРДІОТРИЛУ ТА ЙОГО МЕТАБОЛІТУ
Вступ. Під керівництвом
проф. Мазура І. А. синтезовано вітчизняні препарати, похідні
1,2,4-триазолу: кардіотрил – 1-(β-фенілетил)-4-аміно-(п-диметиламінобензальдегід)-1,2,4-триазолу
бромід та його метаболіт. Кардіотрил
проявляє протиішемічну, вазоділятаторну, мембраностабілізуючу та фібринолітичну
дію, метаболіт характеризується більш швидкою та вираженою лікувальною
активністю [1].
В попередніх дослідженнях кафедри фармакології та
клінічної фармакології Національного медичного університету імені О.О.
Богомольця було проведено прогнозування активності трианолу (кардіотрилу) та його
метаболіту на основі структурних формул за допомогою програми PASS Inet. Згідно комп’ютерного прогнозування
метаболіт кардіотрилу проявляє
властивості, як інгібітор агрегації тромбоцитів, нейропротектор, інгібітор
НАДФ-оксидази, гіпотензивний, церебропротектор, цитопротектор, ангіопротектор.
Перспективними напрямками експериментальних досліджень кардіотрилу та його
метаболіту є встановлення антинеопластичних, протимікробних властивостей, а
також вивчення впливу даних сполук на обмін речовин [11, 12, 14, 15, 19, 21, 22]. В
плані продовження досліджень метою роботи було встановити квантово-хімічні
параметри електронної та просторової структури молекул кардіотрилу
та його метаболіту.
Методи. Для молекул кардіотрилу
та його метаболіту проведено пошук найбільш стабільної конформації методами
молекулярної механіки ММ+ та неемпіричним методом B3LYP/6-31G(d, p) [4, 6, 7, 8, 10]. Методи обрано з урахуванням
даних літератури щодо квантово-хімічних досліджень похідних триазолу [13, 16, 17, 18, 20]. Розраховані показники:
загальні розміри молекул (Å), відстані між атомами (Å); розміри
кутів між зв’язками (°); розподіл електростатичного потенціалу в молекулах;
вільна енергія гідратації (ккал/моль); заряди на атомах (ат. од.); енергії
вищої зайнятої (ВЗМО) і нижчої вакантної (НВМО) молекулярних орбіталей (еВ).
Результати та
обговорення. Триазоли – це органічні сполуки класу гетероциклів, що мають вигляд п’ятичленного
циклу з трьома атомами азоту та двома атомами вуглецю (брутто-формула C2H3N3, молекулярна маса 69,6). Існує два ізомерних триазоли: 1,2,3-триазол та 1,2,4-триазол. Незаміщені або C-заміщені триазоли можуть бути в двох таутомерних формах. Дані сполуки належать до 6π-електронних ароматичних систем [3]. Кардіотрил належить до
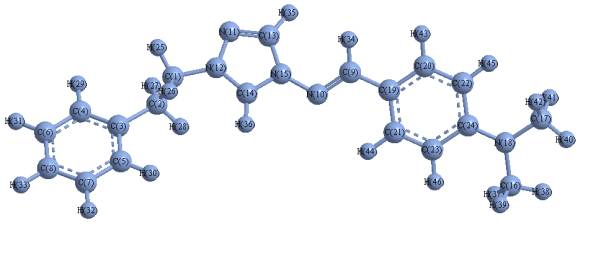
похідних 1,2,4-триазолу, на рис. 1 показана структура молекули в найбільш
стабільній конформації за даними проведених розрахунків.
|
|
|
Рис. 1. Структура
молекули кардіотрилу з позначенням типів атомів та їх номерів, прийнятих при
розрахунках |
Згідно результатів досліджень розміри: молекули кардіотрилу за осями
складають: Х – 5,46 Å; Y – 2,45 Å; Z – 14,94 Å (рис. 1), а
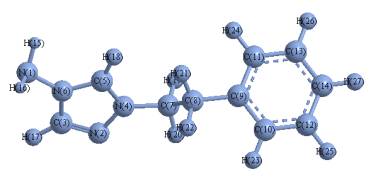
метаболіту кардіотрилу – Х – 3,45 Å; Y – 2,37 Å; Z – 8,96 Å
(рис. 2)
|
|
|
Рис. 2. Структура молекули метаболіту кардіотрилу, з позначенням
типів атомів та їх номерів, прийнятих при розрахунках |
Відстані між атомами та розміри кутів між зв’язками належать до
топологічних дескрипторів фармакологічної активності [9]. Можливість розрізнювати дуже
близькі за будовою та складом сполуки робить топологічні індекси одними з
найбільш розповсюджених молекулярних дескрипторів в QSAR-аналізі. Статистично
достовірні кореляції топологічних дескрипторів з певними видами фармакологічної
активності знаходять застосування при спрямованому пошуку лікарських засобів навіть
у тих випадках, коли логічне пояснення причин таких кореляцій відсутнє.
Міжмолекулярні
взаємодії кардіотрилу в організмі людини можуть бути описані різними якісними
показниками: зарядами на атомах, потенціалами іонізації (енергія ВЗМО),
спорідненістю до електрона (енергія НВМО), індексами реакційної здатності. У таблиці 1 наведені значення зарядів на атомах у молекулі кардіотрилу, у таблиці 2
– у молекулі метаболіту кардіотрилу.
Найбільш
негативні заряди в молекулі кардіотрилу спостерігаються на атомах N18 (-0.49 ат. од.), N10 (-0.35 ат.
од.), N15 (-0.29 ат. од.), N12 (-0.27 ат. од.), C2 (-0.27 ат.
од.). Найбільша
електронна щільність (щільність імовірності знаходження електрона в даній точці
простору) характерна для атомів N10 (191.27), N11 (191.38), N12 (190.61), N15
(190.58), N18 (190.43). Найбільш негативний електростатичний потенціал мають
атоми N10 (-18.20), N11 (-18.17), N12 (-18.09), N15 (-18.08), N18 (-18.20).
Саме ці атоми, як сильні електронодонори в молекулі, можуть бути нуклеофільними
реакційними центрами. Це підтверджується на практиці: триазоли вступають у
реакції електрофільного заміщення по атомам вуглецю та азоту (найбільш
характерними є реакції алкілування та ацетилування). В кислому середовищі
електрофільне заміщення триазолів не відбувається через утворення неактивних
триазолієвих катіонів [3].
Таблиця 1
Заряди, електростатичний потенціал та електронна щільність на атомах кардіотрилу
|
Номер
атома |
Тип атома |
Заряд,
ат.од. |
Електростатичний потенціал, ат.од. |
Електронна щільність,
ат. од. |
|
1.
|
карбон |
0.07 |
-14.56 |
117.61 |
|
2.
|
карбон |
-0.27 |
-14.61 |
117.59 |
|
3.
|
карбон |
0.11 |
-14.64 |
117.65 |
|
4.
|
карбон |
-0.12 |
-14.65 |
117.68 |
|
5.
|
карбон |
-0.12 |
-14.65 |
117.68 |
|
6.
|
карбон |
-0.08 |
-14.66 |
117.68 |
|
7.
|
карбон |
-0.08 |
-14.66 |
117.68 |
|
8.
|
карбон |
-0.08 |
-14.66 |
117.68 |
|
9.
|
карбон |
0.14 |
-14.56 |
117.69 |
|
10.
|
нітроген |
-0.35 |
-18.20 |
191.27 |
|
11.
|
нітроген |
-0.24 |
-18.17 |
191.38 |
|
12.
|
нітроген |
-0.27 |
-18.09 |
190.61 |
|
13.
|
карбон |
0.32 |
-14.51 |
117.60 |
|
14.
|
карбон |
0.39 |
-14.49 |
117.59 |
|
15.
|
нітроген |
-0.29 |
-18.08 |
190.58 |
|
16.
|
карбон |
-0.19 |
-14.61 |
117.53 |
|
17.
|
карбон |
-0.19 |
-14.61 |
117.53 |
|
18.
|
нітроген |
-0.49 |
-18.20 |
190.43 |
|
19.
|
карбон |
0.07 |
-14.63 |
117.59 |
|
20.
|
карбон |
-0.12 |
-14.62 |
117.69 |
|
21.
|
карбон |
-0.10 |
-14.63 |
117.69 |
|
22.
|
карбон |
-0.13 |
-14.64 |
117.63 |
|
23.
|
карбон |
-0.12 |
-14.64 |
117.65 |
|
24.
|
карбон |
0.37 |
-14.58 |
117.62 |
В молекулі метаболіту кардіотрилу найбільш негативні заряди встановлені на
атомах N1 (-0.43 ат. од.), N2 (-0.27 ат.
од.), N4 (-0.28 ат. од.), N6 (-0.34 ат. од.), C8 (-0.29 ат.
од.). Найбільшу
електронну густину та негативний електростатичний потенціал мають атоми всі
атоми нітрогену.
Таблиця 2
Заряди, електростатичний потенціал та електронна щільність на атомах метаболіту кардіотрилу
|
Номер
атома |
Тип атома |
Заряд,
ат.од. |
Електростатичний потенціал, ат.од. |
Електронна щільність,
ат. од. |
|
1.
|
нітроген |
-0.43 |
-18.11 |
190.75 |
|
2.
|
нітроген |
-0.27 |
-18.15 |
191.36 |
|
3.
|
карбон |
0.35 |
-14.47 |
117.64 |
|
4.
|
нітроген |
-0.28 |
-18.04 |
190.61 |
|
5.
|
карбон |
0.42 |
-14.43 |
117.61 |
|
6.
|
нітроген |
-0.34 |
-18.02 |
190.50 |
|
7.
|
карбон |
-0.04 |
-14.53 |
117.59 |
|
8.
|
карбон |
-0.29 |
-14.58 |
117.58 |
|
9.
|
карбон |
0.10 |
-14.62 |
117.67 |
|
10. |
карбон |
-0.13 |
-14.65 |
117.69 |
|
11. |
карбон |
-0.13 |
-14.64 |
117.69 |
|
12. |
карбон |
-0.10 |
-14.66 |
117.68 |
|
13. |
карбон |
-0.10 |
-14.66 |
117.68 |
|
14. |
карбон |
-0.10 |
-14.67 |
117.68 |
Значення
зарядів на атомах лише опосередковано
характеризують особливості поверхні потенційної енергії реагентів в ході
хімічної реакції. Побудова самої поверхні потенційної енергії є складним обчислювальним завданням
і для багатоатомних молекул навіть у значному наближенні
застосовується вкрай рідко. Частіше для
вивчення специфічних міжмолекулярних взаємодій застосовується метод опису
електростатичного потенціалу молекул, так як у багатьох типах взаємодій (іонні,
електро- та нуклеофільні реакції,
утворення водневих зв'язків та донорно-акцепторних комплексів) головну роль
грають електричні Кулонівські взаємодії. Будь-яку молекулу можна представити як
систему ядер з відповідним електронним розподілом в обмеженій області навколо цих ядер. Такій системі позитивних і негативних частинок в
навколишньому просторі молекули буде відповідати
електростатичне поле з різним потенціалом в кожній точці.
Виходячи з цього, молекулярний електростатичний потенціал визначили як енергію електростатичної
взаємодії ядер і електронного розподілу молекули з позитивним одиничним
"пробним" зарядом, розміщеним в заданій точці навколишнього до молекули простору [2, 5, 9].
Величина молекулярного
електростатичного потенціалу є інтегральною характеристикою молекули, тому її
не можна пов'язати з окремим атомом або функціональною групою. Проте, маючи на увазі локалізацію мінімумів поблизу
певного атома, зазвичай пишуть про
електростатичний потенціал даного атома.
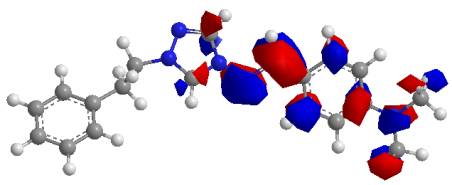
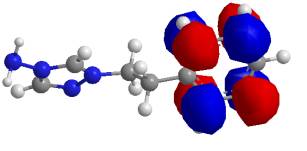
На рис. 3 – 6 показана локалізація граничних орбіталей в молекулах
кардіотрилу та його метаболіту.
|
|
|
Рис. 3. Локалізація ВЗМО в молекулі кардіотрилу |
|
|
|
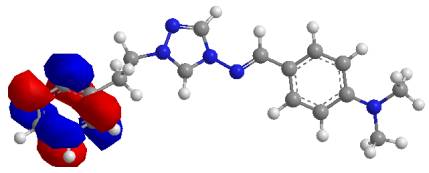
Рис. 4. Локалізація НВМО в молекулі кардіотрилу |
|
|
|
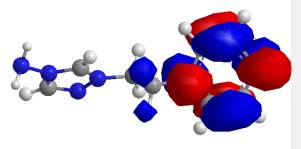
Рис. 5. Локалізація ВЗМО в молекулі метаболіту
кардіотрилу |
|
|
|
Рис. 6. Локалізація НВМО в молекулі метаболіту
кардіотрилу |
ВЗМО характеризує взаємодію молекули з електроноакцепторами, а НВМО – з
електронодонорами. Відповідно до теореми Купменса, енергії граничних орбіталей
відповідають значенням потенціалу іонізації молекули IA (енергія ВЗМО) або її спорідненості
до електрону AA (енергія НВМО).
В молекулі кардіотрилу нараховується 112 молекулярних орбіталей. ВЗМО (№ 62) локалізується на диметиламінобензальдегідному та триазоловому
фрагментах та має енергію -2,238 еВ. НВМО (№ 63) займає фенілетильний фрагмент
та має енергію -1,090 еВ.
В молекулі метаболіту кардіотрилу нараховується 69 молекулярних орбіталей.
ВЗМО (№ 37) має енергію -1,116 еВ, а НВМО (№ 38) -0,641 еВ. Обидві граничні
орбіталі локалізовані на фенілетильному фрагменті.
Вільна енергія гідратації метаболіту кардіотрилу становить -57.47 ккал/моль. Значення цього параметра
вказує на розчинність препарата у воді. При вивченні
взаємодії даного лікарського засобу з будь-якими молекулами або активними
центрами у водному середовищі необхідно враховувати ефекти сольватації,
оскільки енергія взаємодії метаболіту кардіотрилу з молекулами води може перевищувати енергію взаємодій з іншими,
розчиненими
сполуками, тобто утворення відповідних
комплексів, особливо одноцентрових, може бути енергетично невигідним.
Висновки. 1. Найбільші негативні заряди, електронну густину та
електростатичний потенціал в молекулах кардіотрилу та його метаболіту мають
атоми нітрогену. Саме ці атоми, як сильні електронодонори в молекулі, можуть
бути нуклеофільними реакційними центрами. 2. ВЗМО в молекулі кардіотрилу
локалізується на диметиламінобензальдегідному
та триазоловому фрагментах, має енергію -2,238 еВ. НВМО займає фенілетильний фрагмент
та має енергію -1,090 еВ. В молекулі метаболіту кардіотрилу ВЗМО має енергію
-1,116 еВ, а НВМО -0,641 еВ. Обидві граничні орбіталі локалізовані на
фенілетильному фрагменті. 3. Вільна енергія гідратації метаболіту кардіотрилу
становить -57.47 ккал/моль.
ЛІТЕРАТУРА
2.
Грибов Л.А., Муштакова С.П. Квантовая химия: Учебник. – М.: Гардарики,
1999. – 390 с.
3.
Мазур И.А., Волошин Н. А., Чекман И. С. Тиотриазолин. — Львов: Наутилус. –
2005. – 156 с.
7.
Соловьев М.Е., Соловьев М.М. Компьютерная химия. – М.: Солон-пресс, 2005. –
325 с.
12. Aster S.D., Graham D.W.,
Kharbanda D. et al. Bis-aryl triazoles as selective inhibitors of
11beta-hydroxysteroid dehydrogenase type 1 // Bioorg. Med. Chem. Lett. – 2008. – Vol. 1,
№ 18. – P. 2799 – 2804.
13. Avci
D., Atalay
Y., Sekerci
M., Dinçer
M. Molecular structure
and vibrational and chemical shift assignments of
3-(2-hydroxyphenyl)-4-phenyl-1H-1,2,4-triazole-5-(4H)-thione by DFT and ab
initio HF calculations // Spectrochim Acta A Mol Biomol Spectrosc. – 2009. – Vol. 73,
№ 1. – P. 212 – 7.
16. da Silva G., Moore E.E., Bozzelli J.W. Quantum chemical study of the structure and
thermochemistry of the five-membered nitrogen-containing heterocycles and their
anions and radicals // J Phys Chem A. – 2006. – Vol.
110, № 51. – P. 13979 – 88.
17. Dinçer
M., Avci
D., Sekerci
M., Atalay
Y. Molecular structure
and vibrational and chemical shift assignments of
5-(2-Hydroxyphenyl)-4-(p-tolyl)-2,4-dihydro-1,2,4-triazole-3-thione by DFT and
ab initio HF calculations // J Mol Model. – 2008. – Vol. 14,
№ 9. – P. 823 – 32.
18. Guédira F., Castellà-Ventura M., Zaydoun S., Elhajji A., Lautié A., Saidi Idrissi M. Ab initio and density functional study of the
geometrical, electronic and vibrational properties of 3,4'-bi-1,2,4-triazole //
Spectrochim Acta A Mol Biomol Spectrosc. – 2009. – Vol. 73,
№ 4. – P. 738 – 46.
20. Karakurt
T., Dinçer
M., Cetin
A., Sekerci
M. Molecular structure
and vibrational bands and chemical shift assignments of
4-allyl-5-(2-hydroxyphenyl)-2,4-dihydro-3H-1,2,4-triazole-3-thione by DFT and
ab initio HF calculations // Spectrochim Acta A Mol Biomol Spectrosc. – 2010. – Vol. 77,
№ 1. – P. 189 – 98.